题目内容
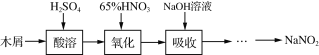
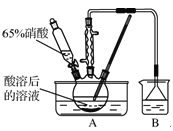
【题目】(1)分析如图所示的三个装置,回答下列问题:

①装置a中铝电极上的电极反应式为________________________。
②装置b中产生气泡的电极为________电极(填“铁”或“铜”),装置c中铜电极上的电极反应式为_____________________________________。
燃料电池是一种高效低污染的新型电池。燃料电池所用燃料可以是氢气,也可以是其他燃料,如甲烷、肼等。
(2)如图是甲烷燃料电池原理示意图,回答下列问题:

①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为:__________________。
②电池工作一段时间后电解质溶液的pH________(填“增大”“减小”或“不变”)。
(3)肼分子(H2N—NH2)可以在氧气中燃烧生成氮气和水,利用肼、氧气与KOH溶液组成碱性燃料电池,请写出该电池反应的负极电极反应式______________________________。
【答案】(1)①Al-3e-+4OH-=AlO2-+2H2O ②铁 O2+2H2O+4e-=4OH-(第2空1分,其余2分)
(2)①a CH4+10OH--8e-=CO32-+7H2O ②减小(第1空1分,其余2分)
(3)N2H4-4e-+4OH-=4H2O+N2↑(2分)
【解析】
试题分析:(1)①装置中金属铝能与氢氧化钠溶液反应,则a中铝电极是负极,正极是镁,则负极上的电极反应式为Al-3e-+4OH-=AlO2-+2H2O。
②装置中常温下铁在浓硝酸中钝化,则铜电极是负极,铁是正极,溶液中的硝酸根在正极得到电子,则b中产生气泡的电极为铁;装置c中铁是负极,铜是正极,发生铁的吸氧腐蚀,则铜电极上的电极反应式为O2+2H2O+4e-=4OH-;
(2)①甲烷失去电子,则甲烷在负极通入,因此电池的负极a电极,该极的电极反应式为CH4+10OH--8e-=CO32-+7H2O。
②由于反应后产生碳酸钠,即电池工作过程中消耗氢氧根,因此电池工作一段时间后电解质溶液的pH减小。
(3)肼在负极发生失去电子的氧化反应,则该电池反应的负极电极反应式为N2H4-4e-+4OH-=4H2O+N2↑。