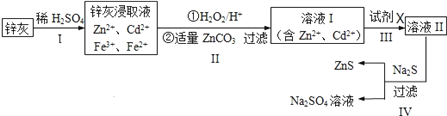
题目内容
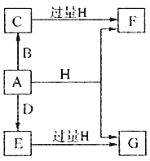
【题目】A、B、D是由常见的短周期非金属元素形成的单质,常温下A是淡黄色粉末,B、D是气体,F、G、H的焰色反应均为黄色,水溶液均显碱性,E有漂白性。它们之间的转化关系如图所示(部分产物及反应条件已略去),回答下列问题:
(1)A所含元素在周期表中的位置为______________,C的电子式为_______________。
(2)A与H在加热条件下反应的化学方程式为__________________。
(3)将A溶于沸腾的G溶液中可以制得化合物I,I在酸性溶液中不稳定,易生成等物质的量的A和E,I在酸性条件下生成A和E的离子方程式为____________________。I是中强还原剂,在纺织、造纸工业中作为脱氯剂,向I溶液中通入氯气可发生反应,参加反应的I和氯气的物质的量比为1:4,该反应的离子方程式为__________________。
(4)向含有0.4molF、0.1molG的混合溶液中加入过量盐酸,完全反应后收集到aL气体C(标准状况),取反应后澄清溶液,加入过量FeCl3溶液,得到沉淀3.2g,则a=____________________。
【答案】 第三周期 第ⅥA族 ![]() 3S + 6NaOH
3S + 6NaOH ![]() 2Na2S + Na2SO3 + 3H2O 2H+ + S2O32-
2Na2S + Na2SO3 + 3H2O 2H+ + S2O32- ![]() S↓+ SO2↑+H2O 4Cl2 +S2O32-+ 5H2O
S↓+ SO2↑+H2O 4Cl2 +S2O32-+ 5H2O![]() 8Cl- + 2SO42- + 10H+ 2.24
8Cl- + 2SO42- + 10H+ 2.24
【解析】常温下A是淡黄色粉末,且为单质,则A是硫;B、D是气体,A和D生成E,E有漂白性,说明E为SO2,D是O2,则B是H2,C为H2S,F、G、H的焰色反应均为黄色,F、G、H中均含有钠元素,水溶液均显碱性,SO2和H2S均能与H反应,H为NaOH,则F为Na2S,G为Na2SO3,(1)A是硫单质,位于第三周期ⅥA元素,C为H2S,属于共价化合物,其电子式为![]() ;(2)硫单质与热的氢氧化钠溶液发生歧化反应,生成硫化钠和亚硫酸钠,即反应方程式为:3S + 6NaOH
;(2)硫单质与热的氢氧化钠溶液发生歧化反应,生成硫化钠和亚硫酸钠,即反应方程式为:3S + 6NaOH ![]() 2Na2S + Na2SO3 + 3H2O;(3)S和沸腾Na2SO3得到化合物Na2S2O3,Na2S2O3在酸性条件下生成S和SO2,即离子反应方程式为:2H+ + S2O32-
2Na2S + Na2SO3 + 3H2O;(3)S和沸腾Na2SO3得到化合物Na2S2O3,Na2S2O3在酸性条件下生成S和SO2,即离子反应方程式为:2H+ + S2O32- ![]() S↓+ SO2↑+H2O,氯气具有强氧化性,能把S2O32-氧化成SO42-,本身被还原成Cl-,Na2SO3和氯气的物质的量之比为1:4,即两者的系数为1:4,S2O32-+4Cl2→2SO42-+8Cl-,根据化学反应方程式原子个数守恒,反应前少5个O,即缺少5molH2O,则生成物中应有10H+,其离子反应方程式为4Cl2+S2O32-+5H2O=8Cl-+2SO42-+10H+;(4)反应后澄清溶液,加入过量FeCl3溶液,得到沉淀3.2g,根据反应2Fe3++S2-=2Fe2++S↓,该反应中消耗的Na2S为0.1mol;Na2S与Na2SO3的混合溶液中加入过量盐酸,发生反应:2S2-+SO32-+6H+=3S↓+3H2O,消耗Na2SO3 0.1mol,剩余的Na2S 0.1mol与盐酸反应放出H2S,放出H2S的物质的量为0.1mol,标准状况下的体积为2.24L。
S↓+ SO2↑+H2O,氯气具有强氧化性,能把S2O32-氧化成SO42-,本身被还原成Cl-,Na2SO3和氯气的物质的量之比为1:4,即两者的系数为1:4,S2O32-+4Cl2→2SO42-+8Cl-,根据化学反应方程式原子个数守恒,反应前少5个O,即缺少5molH2O,则生成物中应有10H+,其离子反应方程式为4Cl2+S2O32-+5H2O=8Cl-+2SO42-+10H+;(4)反应后澄清溶液,加入过量FeCl3溶液,得到沉淀3.2g,根据反应2Fe3++S2-=2Fe2++S↓,该反应中消耗的Na2S为0.1mol;Na2S与Na2SO3的混合溶液中加入过量盐酸,发生反应:2S2-+SO32-+6H+=3S↓+3H2O,消耗Na2SO3 0.1mol,剩余的Na2S 0.1mol与盐酸反应放出H2S,放出H2S的物质的量为0.1mol,标准状况下的体积为2.24L。

【题目】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标准状况) | 100 | 240 | 464 | 576 | 620 |
①哪一时间段时间段反应速率最大______min(填0~1、1~2、2~3、3~4、4~5),原因是____________。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率__________(设液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入等体积的下列溶液以减慢反应速率,你认为不可行的是__________。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)在一定温度下,将一定量的气体通入体积为2 L的密闭容器中,使其发生反应,有关物质X、Y、Z的物质的量的变化如图所示。

①则下列有关推断正确的是________________。
A.该反应的化学方程式是:3Z![]() 3X+2Y
3X+2Y
B.t0时,X、Y、Z的质量不再改变
C.t0时,Z的浓度为1.2 mol/L
D.t0时反应停止,反应速率为0
②t0时,Z的转化率为_____________。
③若t0=2min,则2min内用Y的浓度变化表示的反应速率为:________________。
【题目】氢气是一种新型的绿色能源,又是一种重要的化工原料。以生物材质(以C 计)与水蒸气反应制取H2是一种低耗能,高效率的制H2方法。该方法由气化炉制造H2和燃烧炉再生CaO两步构成。气化炉中涉及到的反应为:
I.C(s)+H2O(g)![]() CO(g)+H2(g) K1;
CO(g)+H2(g) K1;
Ⅱ.CO(g)+H2O(g)![]() CO2(g)+H2(g) K2;
CO2(g)+H2(g) K2;
Ⅲ.CaO(s)+CO2(g)![]() CaCO3(s) K3;
CaCO3(s) K3;
(1)该工艺制H2总反应可表示为C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g),其反应的平衡常数K=_______________(用K1、K2、K3的代数式表示)。在2L的密闭容器中加入一定量的C(s)、H2O(g)和CaO(s)。下列能说明反应达到平衡状态的是__________。
CaCO3(s)+2H2(g),其反应的平衡常数K=_______________(用K1、K2、K3的代数式表示)。在2L的密闭容器中加入一定量的C(s)、H2O(g)和CaO(s)。下列能说明反应达到平衡状态的是__________。
a.容器内混合物的质量不变 b.H2与H2O(g)的物质的量之比不再变化
c.混合气体的密度不再变化 d.形成 a mol H-H键的同时断裂 2 amol H-O键
(2)对于反应Ⅰ,不同温度和压强对H2产率影响如下表。
压强 温度 | p1/Mpa | p2/Mpa |
500℃ | 45.6% | 51.3% |
700℃ | 67.8% | 71.6% |
由表中数据判断:p1 ______ p2(填“>”、“<”或“=”)
下列图像正确的是_________。
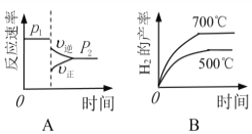
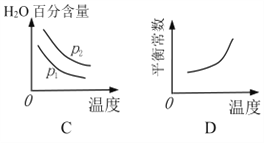
(3)已知反应Ⅱ的△H= -41.1 kJ/mol, C=O、O-H、H-H的键能分别为803kJ/mol,464 kJ/mol、436 kJ/mol,则 CO中碳氧键的键能为___________ kJ/mol。
(4)对于反应Ⅲ,若平衡时再充入CO2,使其浓度增大到原来的2倍,则平衡向_____________(填“正反应”、“逆反应”)方向移动;当重新平衡后,CO2浓度_________(填“变大”、“变小”或“不变”)。