题目内容
【题目】研究苯酚与FeCl3溶液的显色反应,实验如下。下列说法不正确的是
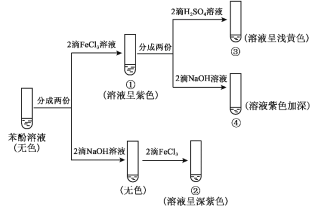
A.对比①③中的现象,说明滴加稀硫酸后,c(Fe3+)变小
B.向试管②中滴加硫酸至过量,溶液颜色变为浅黄色
C.对比①②、①④中的现象,说明紫色物质的生成与溶液中 c(C6H5O)相关
D.对比①②、①④中的现象,说明结合C6H5O的能力:H+>Fe3+
【答案】A
【解析】
A.①中溶液为紫色,③中溶液为浅黄色,可知滴加稀硫酸后,c(Fe3+)增大,故A错误;
B.加硫酸,酸性增强,使平衡Fe3++6C6H5OH![]()
![]() +3H+逆向移动,溶液颜色变为浅黄色,故B正确;
+3H+逆向移动,溶液颜色变为浅黄色,故B正确;
C.对比①②、①④中的现象,平衡正向进行程度越大,紫色越深,则紫色物质的生成与溶液中 c(C6H5O-)相关,故C正确;
D.苯酚溶液中滴加FeCl3溶液后溶液中存在Fe3++6C6H5OH![]()
![]() +3H+,比较①②,①是苯酚与氯化铁溶液反应,而②则是苯酚钠溶液与等量的氯化铁溶液,但是①的颜色不如②的深,说明①中
+3H+,比较①②,①是苯酚与氯化铁溶液反应,而②则是苯酚钠溶液与等量的氯化铁溶液,但是①的颜色不如②的深,说明①中![]() 的浓度不如②的大,故说明H+结合C6H5O的能力>Fe3+,比较可知①的颜色比④的浅,是由于④中加入了NaOH溶液,消耗了H+,使Fe3++6C6H5OH
的浓度不如②的大,故说明H+结合C6H5O的能力>Fe3+,比较可知①的颜色比④的浅,是由于④中加入了NaOH溶液,消耗了H+,使Fe3++6C6H5OH![]()
![]() +3H+平衡正向移动,故说明溶液中H+结合C6H5O的能力>Fe3+,故D正确;
+3H+平衡正向移动,故说明溶液中H+结合C6H5O的能力>Fe3+,故D正确;
故答案为:A。

 阅读快车系列答案
阅读快车系列答案【题目】实验是化学学习中非常重要的内容,根据下面两个实验回答问题。
(一)某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
(查阅资料)25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
(实验探究)向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀。
(1)分别向两支试管中加入不同试剂,记录实验现象如表:(表中填空填下列选项中字母代号)
试管编号 | 加入试剂 | 实验现象 |
Ⅰ | 2滴0.1mol/LFeCl3溶液 | ①_____ |
Ⅱ | 4mL2mol/LNH4Cl溶液 | ②_____ |
A.白色沉淀转化为红褐色沉淀 B.白色沉淀不发生改变
C.红褐色沉淀转化为白色沉淀 D.白色沉淀溶解,得无色溶液
(2)同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。
猜想2:____________________________________________________________。
(3)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明猜想正确的是____(填 “1”或“2”)。
(二)测定某品牌的碘盐(含有碘酸钾)中碘元素的百分含量。准确称取5.000 0 g该碘盐,溶于蒸馏水,然后与足量的KI溶液在酸性条件下混合(发生的反应为KIO3+3H2SO4+5KI===3K2SO4+3I2+3H2O),充分反应后将混合溶液稀释至250 mL,然后取25.00 mL用5.0×10-4 mol·L-1的Na2S2O3标准溶液进行滴定(用淀粉作指示剂,反应为I2+2S2O32-===2I-+S4O62-)。有关实验数值如下表所示。
滴定次数 | 待测液的体积(mL) | 滴定前的读数(mL) | 滴定后的读数(mL) |
第一次 | 25.00 | 0.00 | 15.90 |
第二次 | 25.00 | 0.00 | 14.99 |
第三次 | 25.00 | 0.00 | 15.01 |
该碘盐中碘元素的百分含量为________。(保留三位有效数字)下列操作中,会导致所测得的碘元素的百分含量偏大的是________。
a.滴定终时,俯视刻度
b.没有用Na2S2O3标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水