题目内容
16.在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是( )| A. | n(Cl2):n(Fe)=5:4 5Cl2+4Fe $\frac{\underline{\;点燃\;}}{\;}$2FeCl2+2FeCl3 | |
| B. | n(Cl2):n(FeBr2)=1:1 Fe2++2Br-+Cl2═Fe3++Br2+2Cl- | |
| C. | n(MnO4-):n(H2O2)=2:3 2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | |
| D. | n(Fe):n[HNO3(稀)]=1:3 4Fe+12H++3NO3-═3Fe2++Fe3++3NO↑+6H2O |
分析 A.铁与氯气反应生成氯化铁,与反应物用量无关;
B.二价铁离子还原性强于溴离子,二者等物质的量反应,二价铁离子全部被氧化,溴离子只氧化一半;
C.n(MnO4-):n(H2O2)=2:3,双氧水全部被氧化;
D.n(Fe):n(HNO3(稀))═1:3,反应生成亚铁离子和铁离子.
解答 解:A.铁与氯气反应生成氯化铁,化学方程式:3Cl2+2Fe $\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故A错误;
B.n(Cl2):n(FeBr2)=1:1,反应的离子方程式:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl-,故B错误;
C.n(MnO4-):n(H2O2)=2:3,双氧水被氧化成氧气,方程式中一定满足:n(H2O2)=n(O2),正确的离子方程式为:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故C错误;
D.n(Fe):n(HNO3(稀))═1:3,反应生成亚铁离子和铁离子,反应的离子方程式为:4Fe+12H++3NO3-=3Fe2++Fe3++3NO↑+6H2O,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意反应物用量对反应的影响,题目难度较大.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案
相关题目
6.下列化学方程式中,书写不正确的是( )
| A. | 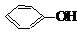 +NaOH→ +NaOH→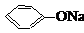 +H2O +H2O | B. | 2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ | ||
| C. | CH2=CH2+H2O→CH3CH2OH | D. | CH4+Cl2→CH2Cl2+H2 |
5.M、N、X、Y四种物质有如下转化关系,M$→_{反应①}^{X}$N$→_{反应②}^{X}$Y(反应条件和其他产物已省略),下列选项不可能的是( )
| A. | M:Na X:O2 | B. | M:IINO3 X:Fe | C. | M:NH3 X:O2 | D. | M:Al X:NaOH |
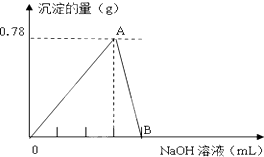 向20mLAlCl3溶液中滴入2mol•L-1NaOH溶液时,沉淀质量与所滴加NaOH溶液体积(mL)关系如图所示:
向20mLAlCl3溶液中滴入2mol•L-1NaOH溶液时,沉淀质量与所滴加NaOH溶液体积(mL)关系如图所示: