题目内容
【题目】如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体。根据图示回答问题:
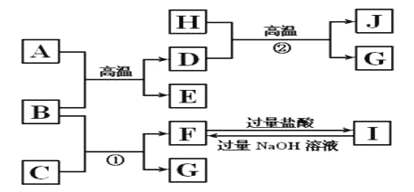
(1)写出下列物质的化学式:A________, I________,
(2)反应反应②的化学方程式是__________________;
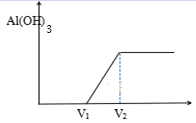
(3)如右图所示,将I持续滴加入NaOH中开始没有沉淀生成,后来出现白色沉淀,V1:V2=_________;
(4)3molJ与足量的稀硝酸反应生成____________molNO。
【答案】 Fe2O3 AlCl3 3Fe+4H2O(g) ![]() Fe3O4+4H2 3:4 1mol
Fe3O4+4H2 3:4 1mol
【解析】因为B是地壳中含量最高的金属元素,即B为Al;J是磁性材料即J为Fe 3 O 4 。又D+H![]() Fe 3 O 4 +G,且D是单质,G是气体单质,所以D应为Fe,G为H 2 ,H为H 2 O;因为A+Al
Fe 3 O 4 +G,且D是单质,G是气体单质,所以D应为Fe,G为H 2 ,H为H 2 O;因为A+Al![]() Fe+E,即此反应为铝热反应,一般情况下A为Fe 2 O 3 ;因为F
Fe+E,即此反应为铝热反应,一般情况下A为Fe 2 O 3 ;因为F![]() I,而F中又含有Al元素,所以F为NaAlO 2 、I为AlCl 3 ,则C为NaOH。这样就很容易得出个小题的答案为:
I,而F中又含有Al元素,所以F为NaAlO 2 、I为AlCl 3 ,则C为NaOH。这样就很容易得出个小题的答案为:
(1)写出下列物质的化学式:A为Fe 2 O 3 ,I为AlCl 3 ;
(2)反应①的化学方程式是2Al+NaOH+2H 2 O=2NaAlO 2 +3H 2 ↑;
反应②的化学方程式是3Fe+4H 2 O![]() Fe 3 O 4 +3H 2 ;
Fe 3 O 4 +3H 2 ;
(3)Al3++4OH—= AlO2— +2H2O,3AlO2— +Al3++6H2O =4Al(OH)3↓,由方程式计量比例关系可以得到V1:V2=3:4;
(4)3molJ (Fe 3 O 4)与足量的稀硝酸反应失去3mol电子,1molHNO3转化为NO得3mol电子,所以生成NO为1mol.

 阅读快车系列答案
阅读快车系列答案【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如表:下列说法正确的是( )
2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如表:下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 该温度下此反应的平衡常数K=1.44
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
D. 0~2min的平均速率ν(Z)=2.0×10﹣3molL﹣1min﹣1
