题目内容
【题目】实验室从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
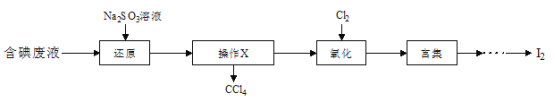
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为_____________________;该操作将I2还原为I-的 目的是__________________。
(2)操作X的名称为 ________________。
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如右图所示)。实验必须控制在较低温度下进行的原因是 ;仪器a、b的名称分别为:a__________、b__________;仪器b中盛放的溶液为__________________。

(4)已知二氧化氯为黄绿色易溶于水的气体,是高效、低毒的消毒剂和水处理剂。现用ClO2氧化酸性含I-废液以回收碘。
①写出ClO2氧化I-的离子方程式 ;
②若处理含相同物质的量的I-酸性废液以回收碘,所需Cl2的物质的量是ClO2的_________倍。
【答案】
(1)SO32- + I2 + H2O = 2I- + SO42- + 2H+;使CCl4中的碘进入水层;
(2)分液;
(3)使氯气在溶液中有较大的溶解度(或防止I2升华或防止I2进一步被氧化);球形冷凝管;锥形瓶;NaOH溶液;
(4)① 2 ClO2 + 10 I—+ 8H+ = 5 I2 + 2 Cl— + 4H2O; ② 2.5;
【解析】
试题分析:(1)碘具有氧化性,能氧化亚硫酸钠生成硫酸钠,自身被还原生成碘离子,离子反应方程式为SO32-+I2+H2O=2I-+2H++SO42-;碘微溶于水,而碘离子易溶于水,为了使更多的I元素进入水溶液应将碘还原为碘离子;故答案为:SO32-+I2+H2O=2I-+2H++SO42-;使CCl4中的碘进入水层;
(2)四氯化碳属于有机物,水属于无机物,二者不互溶,分离互不相溶的液体采用分液的方法分离,所以分离出四氯化碳采用分液的方法;故答案为:分液;
(3)碘易升华,且氯气的溶解度随着温度的升高而减小,温度越高,氯气的溶解度越小,反应越不充分,所以应该在低温条件下进行反应;仪器a为球形冷凝管、b为锥形瓶;氯气、碘蒸气都有毒,不能直接排空,且都能和氢氧化钠溶液反应生成无毒物质,所以用NaOH溶液吸收氯气和碘蒸气,故答案为:使氯气在溶液中有较大的溶解度(或防止碘升华或防止碘进一步被氧化);球形冷凝管;锥形瓶;NaOH溶液;
(4)①用ClO2氧化酸性含I-废液回收碘,是二氧化氯在酸溶液中氧化碘离子生成碘单质,二氧化氯被还原为氯离子,ClO2~Cl-~5e-,2I-~I2~2e-,反应的离子方程式为2ClO2+10I-+8H+=5I2+2Cl-+4H2O,故答案为:2 ClO2 + 10 I—+ 8H+ = 5 I2 + 2 Cl— + 4H2O;
②由氧化还原反应电子守恒,每摩尔Cl2得到2mol电子,而每摩尔ClO2得到5mol电子,则所需Cl2的物质的量是ClO2的2.5倍,故答案为:2.5。

【题目】活性炭可处理大气污染物NO。T℃时,在1L密闭容器中加入NO气体和炭粉,发生反应生成两种气体A和B,测得各物质的物质的量如下:
活性炭/mol | NO/mol | A/mol | B/mol | |
起始状态 | 2.030 | 0.100 | 0 | 0 |
2 min时 | 2.000 | 0.040 | 0.030 | 0.030 |
(1)2 min内,用NO表示该反应的平均速率v(NO)= mol·L-1·min-1;
(2)该反应的化学方程式是________________________________________;
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是_____ 。
①v(NO)∶v(A)∶v(B)=2∶1∶1
②混合气体的密度不再改变
③总压强不再改变
④混合气体的平均相对分子质量不再改变
(4)碳元素可形成数量众多,分布极广的有机化合物,其中甲醇是常见的燃料,甲醇燃料电池的结构示意图如下,一极通入甲醇,另外一极通入氧气;电解质溶液是稀硫酸,电池工作时总反应式:2CH3OH+3O2=2CO2+4H2O。

①a处通入的物质是____,电极反应式为:______;
②b处电极反应式为_________________________;
③电池工作时H+由 极移向 极(填正、负极)。