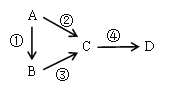
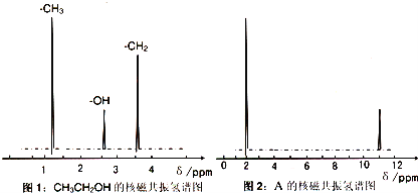
题目内容
【题目】氯化铵被广泛用于医药、干电池、织物印染、洗涤等领域。氯化铵T1温度下有以下平衡:![]()
(1)N原子最外层电子有______种运动状态;上述平衡中物质,在晶体时属于离子晶体的是__________。
(2)![]() 的电子式为______________。
的电子式为______________。
(3)Cl的非金属性强于S,用原子结构的知识说明理由:_________________。
(4)上述该反应的平衡常数表达式为____________________________________。
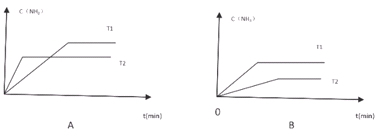
(5)在2L密闭容器中建立平衡,不同温度下氨气浓度变化正确的是_________。
(6)T1温度在2L,容器中,当平衡时测得![]() 为amol/L,保持其他条件不变,压缩容器体积至1L(各物质状态不变),重新达到平衡后测得
为amol/L,保持其他条件不变,压缩容器体积至1L(各物质状态不变),重新达到平衡后测得![]() 为bmol/L。试比较a与b的大小a_____b(填“>”“<”或“=”),并说明理由:___________。
为bmol/L。试比较a与b的大小a_____b(填“>”“<”或“=”),并说明理由:___________。
【答案】5种 ![]()
![]() 氯原子结构与硫原子电子层数相同,但氯原子比硫原子多一个电子,原子半径氯原子小,更容易得到电子,因此氯元素的非金属性比硫强
氯原子结构与硫原子电子层数相同,但氯原子比硫原子多一个电子,原子半径氯原子小,更容易得到电子,因此氯元素的非金属性比硫强 ![]() B = 因为
B = 因为![]() ,始终
,始终![]() ,温度不变,K不变,所以
,温度不变,K不变,所以![]()
【解析】
根据核外电子排布规律分析原子核外电子的运功状态;根据物质的组成及性质分析判断晶体类型;根据共价化合物的成键特点书写电子式;根据反应方程式书写平衡常数表达式,根据勒夏特列原理分析判断平衡的移动方向。
(1)N原子最外层电子排布式为2s22p3,s轨道上的2个电子自旋相反,运动状态不同,p轨道有3种方向,所以有3种运动状态,即N原子最外层电子共有5种运动状态;上述平衡中物质,NH3和HCl常温下为气态,属于分子晶体,NH4Cl为离子化合物,在固态时属于离子晶体,故答案为:5;NH4Cl;
(2)NH3中N原子与H原子以共价键结合,电子式为![]() ;
;
(3)由于氯原子结构与硫原子电子层数相同,但氯原子比硫原子多一个电子,原子半径氯原子小,更容易得到电子,因此氯元素的非金属性比硫强;
(4)化学平衡常数表达式为各生成物浓度的化学计量数次幂的乘积与各反应物浓度的化学计量数次幂的乘积的比值,则上述该反应的平衡常数表达式为![]() ;
;
(5)A图中,T2时先达到平衡,温度越高,反应越快,则T2大于T1,上述反应为吸热反应,则升高温度,平衡向正方向移动,c(NH3)应增大,所以A图错误;B图中T1先达到平衡,说明T1大于T2,升高温度时,平衡向正方向移动,c(NH3)增大,所以B图正确,故答案为B;
(6)因为![]() ,始终c(NH3)=c(HCl),温度不变,K不变,所以
,始终c(NH3)=c(HCl),温度不变,K不变,所以![]() 。
。

【题目】某工业流程中,进入反应塔的混合气体中![]() 和
和![]() 物质的量百分含量分别是10%和6%,发生反应为:
物质的量百分含量分别是10%和6%,发生反应为:![]() ,在其他条件相同时,测得试验数据如下:
,在其他条件相同时,测得试验数据如下:
压强( | 温度(℃) | NO达到所列转化率所需时间(s) | ||
50% | 90% | 98% | ||
1.0 | 30 | 12 | 250 | 2830 |
90 | 25 | 510 | 5760 | |
8.0 | 30 | 0.2 | 3.9 | 36 |
90 | 0.6 | 7.9 | 74 | |
根据表中数据,下列说法正确的是
A.温度越高,越有利于NO的转化
B.增大压强,反应速率变慢
C.在![]() 、90℃条件下,当转化率为98%时反应已达平衡
、90℃条件下,当转化率为98%时反应已达平衡
D.如进入反应塔的混合气体为![]() ,如速率
,如速率![]() 表示,则在
表示,则在![]() 、30℃条件下,转化率从50%增至90%时段,NO的反应速率为
、30℃条件下,转化率从50%增至90%时段,NO的反应速率为![]()