题目内容
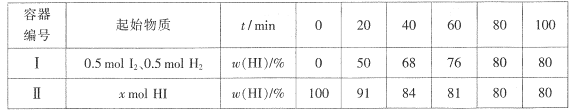
【题目】Boderlscens研究反应:H2(g)+I2(g) ![]() 2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:
2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:
研究发现上述反应中![]() 其中
其中![]() 为常数。下列说法正确的是
为常数。下列说法正确的是
A. 温度为T时该反应的![]()
B. 容器I中前20 min的平均速率v(HI)=0.0125mol.L-1.min-1
C. 若起始时,向容器I中加入物质的量均为0.l mol的H2、I2、HI,反应逆向进行
D. 若两容器中![]() 且
且 ![]() 则x的值一定为1
则x的值一定为1
【答案】AD
【解析】A. 温度为T时该反应的![]() =
= =
=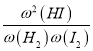 =
=![]() =64,选项A正确;B. 容器I中前20 min
=64,选项A正确;B. 容器I中前20 min ![]() =50%,则物质的量为 0.5mol,故平均速率v(HI)=
=50%,则物质的量为 0.5mol,故平均速率v(HI)=  =0.025mol.L-1.min-1,选项B错误;C. 容器I平衡时H2、I2、HI浓度分别为0.1mol/L、0.1mol/L、0.8mol/L,
=0.025mol.L-1.min-1,选项B错误;C. 容器I平衡时H2、I2、HI浓度分别为0.1mol/L、0.1mol/L、0.8mol/L, ![]() ,若起始时,向容器I中加入物质的量均为0.l mol的H2、I2、HI,
,若起始时,向容器I中加入物质的量均为0.l mol的H2、I2、HI, ![]() ,正反应速率大于逆反应速率,平衡正向进行,选项C错误;D. 若两容器中
,正反应速率大于逆反应速率,平衡正向进行,选项C错误;D. 若两容器中![]() 且
且 ![]() 则为恒容条件下的等效平衡,则x的值一定为1,选项D正确。答案选AD。
则为恒容条件下的等效平衡,则x的值一定为1,选项D正确。答案选AD。

 阅读快车系列答案
阅读快车系列答案【题目】已知 Fe2O3(s)+3CO(g)2Fe(s)+3CO2(g) 在不同温度下的平衡常数如表:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 42.9 | 50.7 | 64.0 |
请回答下列问题:
(1)该反应的平衡常数表达式 K= , △H0(填“>”、“<”或“=”).
(2)在一个容积为10L的密闭容器中,1300℃时加入 Fe、Fe2O3、CO、CO2各1mol,反应经过10min 后达到平衡.求该时间范围内反应的平均反应速率 v(CO2)= , CO 的平衡转化率为 .
(3)欲提高(2)中CO的平衡转化率,可采取的措施是 .
A.增加Fe2O3的量
B.加入合适的催化剂
C.移出部分CO2
D.提高反应温度.