题目内容
【题目】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
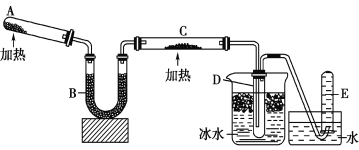
(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是________________。
(2)B中加入的是碱石灰,其作用是_______________________________。
(3)实验时在C中观察到的现象是________________________________。发生反应的化学方程式是:______________________________。
(4)D中收集到的物质是____________,检验该物质的方法和现象是_______________________________。
【答案】2NH4Cl+Ca(OH)2![]() 2NH3↑+2H2O+CaCl2 除去氨气中的水蒸气 黑色粉末逐渐变为红色 3CuO+2NH3
2NH3↑+2H2O+CaCl2 除去氨气中的水蒸气 黑色粉末逐渐变为红色 3CuO+2NH3![]() 3Cu+N2+3H2O 氨水 用红色石蕊试纸检验,试纸变蓝(或用酚酞溶液检验,酚酞溶液变红)
3Cu+N2+3H2O 氨水 用红色石蕊试纸检验,试纸变蓝(或用酚酞溶液检验,酚酞溶液变红)
【解析】
(1)在加热的条件下Ca(OH)2和NH4Cl反应生成氨气、氯化钙和水,据此书写;
(2)根据氨气中含有水蒸气分析碱石灰的作用;
(3)在加热的条件下氨气与氧化铜反应生成铜、氮气和水,据此判断;
(4)氨气和水混合形成氨水,据此分析。
(1)依据题中生成氨气的反应原理可知,氯化铵与氢氧化钙在加热的条件下反应生成氯化钙、水和氨气,反应的化学方程式为2NH4Cl+Ca(OH)2![]() 2NH3↑+2H2O+CaCl2;
2NH3↑+2H2O+CaCl2;
(2)制得的氨气中含有杂质水蒸气,会干扰氨气与氧化铜的反应,可以用碱石灰来吸收,所以B中加入的是碱石灰,其作用是除去氨气中的水蒸气;
(3)氨气和氧化铜在加热的条件下发生反应生成金属铜、水以及氮气,所以反应现象是:黑色粉末逐渐变为红色,发生反应的化学方程式是3CuO+2NH3![]() 3Cu+3H2O+N2;
3Cu+3H2O+N2;
(4)氨气还原氧化铜之后,剩余的气体中有氨气、水蒸气和氮气,在D装置冷凝时氨气和产生的水蒸气会形成氨水,只有氮气不溶于水,故E中收集到的物质是N2,D中收集到的物质是氨水,检验该物质的方法和现象是用红色石蕊试纸检验,试纸变蓝(或用酚酞溶液检验,酚酞溶液变红)。

【题目】完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是( )
|
|
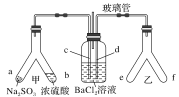
A.用CCl4提取溴水中的Br2 | B.从KI和I2的固体混合物中回收I2 |
|
|
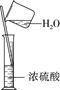
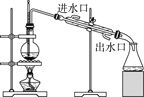
C.稀释浓硫酸 | D.工业酒精制备无水酒精 |
A. A B. B C. C D. D