题目内容
二元酸H2A在水中发生电离:H2A=H++HA-和HA-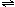 H++A2-,则下列几种物质的水溶液中关系式不正确的是
H++A2-,则下列几种物质的水溶液中关系式不正确的是
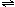 H++A2-,则下列几种物质的水溶液中关系式不正确的是
H++A2-,则下列几种物质的水溶液中关系式不正确的是| A.NaHA:c(Na+)>c(HA-)>c(OH-)>c(H+) |
| B.NaHA:c(Na+)=c(A2-)+c(HA-) |
| C.Na2A:c(Na+)>c(A2-) >c(OH-)>c(H+) |
| D.H2A:c(H+)=c(HA-)+2 c(A2-)+c(OH-) |
A
根据电离方程式可知,该酸的第一步是完全电离的,而第二步是不完全的,存在电离平衡。所以HA-只能电离,而不能水解,溶液是显酸性的,A不正确。根据原子守恒可知,B是正确的。Na2A水解显碱性,C正确。根据电荷守恒中D也是正确的。答案选A。

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目


 NH4++OH- ②HCO3- + H2O
NH4++OH- ②HCO3- + H2O HCO3—+OH—平衡。下列说法不正确的是
HCO3—+OH—平衡。下列说法不正确的是 增大
增大 ,溶液pH减小
,溶液pH减小 减小
减小