题目内容
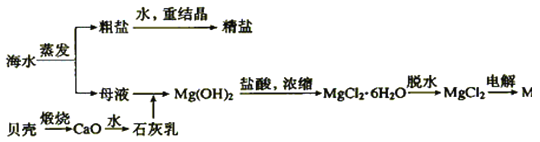
【题目】Pd/A12O3是常见的汽车尾气催化剂。一种从废Pd/A12O3纳米催化剂(主要成分及含量:Pd0.3%,γ-A12O392.8%,其他杂质6.0%)中回收金属Pd的工艺:

已知:γ-Al2O3能与酸反应,α-A12O3不与酸反应。
回答下列问题:
(1)“预处理”时,γ-A12O3经焙烧转化为α-A12O3,该操作的主要目的是_________。
(2)“酸浸”时,Pd转化为PdCl42-,其离子方程式为_________。
(3)“滤液①”和“滤液②”中都含有的主要溶质有_________(填化学式)。
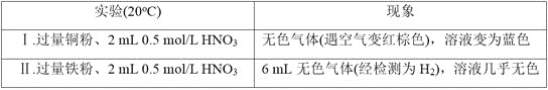
(4)“粗Pd”溶解时,可用稀HNO3替代NaClO3,但缺点是_________。两者相比,_________(填化学式)的氧化效率更高(氧化效率以单位质量得到的电子数表示)。
(5)“沉淀”时,[Pd(NH3)4]2+转化为[Pd(NH3)2]Cl2沉淀,其化学方程式为_________。
(6)酸性条件下,BrO3-能在负载Pd/A12O3纳米催化剂的电极表面快速转化为Br-。
①发生上述转化反应的电极应接电源的_________极(填“正”或“负”);
②研究表明,电流密度越大,电催化效率越高;但当电流密度过大时,该电极会发生副反应生成_________填化学式)。
【答案】有利于Pd与Al2O3的分离 3Pd+ClO3-+6H++11Cl=3PdCl42-+3H2O AlCl3 对环境产生较大污染(或耗酸量大、或腐蚀性强、或氧化效率低) NaClO3 [Pd(NH3)4]Cl2+2HCl=[Pd(NH3)2]Cl2↓+2NH4Cl 负 H2
【解析】
废Pd/A12O3纳米催化剂(主要成分及含量:Pd 0.3%,γ-A12O3 92.8%,其他杂质6.0%)进行预处理,废催化剂进行焙烧,使大量的γ-A12O3经焙烧转化为α-A12O3,处理后,加入足量盐酸和NaClO3进行酸浸和氧化处理,Pd转化为PdCl42-,γ-A12O3转化为Al3+后过滤,发生的离子反应为:3Pd+ClO3-+6H++11Cl=3PdCl42-+3H2O,A12O3+6H+=2Al3++ 3H2O,α-A12O3不与酸反应,对酸浸后的溶液过滤,α-A12O3以滤渣的形式除去,得到含有PdCl42-、Al3+的滤液,向滤液中加入过量的Al单质,将PdCl42-置换为Pb单质,在进行过滤,得到主要含有Al3+、Cl-的滤液①,得到的固体主要含有Pb和过量的Al单质,再加入盐酸将过量的单质Al除去,再次过滤,得到主要含有Al3+、Cl-、H+的滤液②和粗Pd,向粗Pd中再次加入盐酸和NaClO3,将Pd溶解转化为PdCl42-,向得到的溶液中加入氨水,将PdCl42-转化为[Pd(NH3)4]2+,再加入盐酸,使[Pd(NH3)4]2+转化为[Pd(NH3)2]Cl2沉淀,过滤后,对[Pd(NH3)2]Cl2进行焙烧生成高纯度的Pd单质,据此分析解答。
(1)由于α-A12O3不与酸反应,“预处理”时,γ-A12O3经焙烧转化为α-A12O3,该操作的主要目的是将大量的A12O3在酸浸时以沉淀的形式除去,有利于Pd与Al2O3的分离;
(2)根据分析,“酸浸”时,Pd转化为PdCl42-,其离子方程式为3Pd+ClO3-+6H++11Cl=3PdCl42-+3H2O;
(3)根据分析“滤液①”主要含有Al3+、Cl-,“滤液②”中主要含有Al3+、Cl-、H+,二者都含有的主要溶质有AlCl3;
(4)“粗Pd”溶解时,可用稀HNO3替代NaClO3,但缺点是使用硝酸作氧化剂会生成氮氧化物,对环境产生较大污染(或耗酸量大、或腐蚀性强、或氧化效率低);63g硝酸为1mol做氧化剂转化为二氧化氮,转移1mol电子,即1g硝酸参与反应得到![]() mol≈0.016mol的电子,106.5g NaClO3为1mol,做氧化剂转化为PdCl42-,转移6mol电子,即1g NaClO3参与反应得到
mol≈0.016mol的电子,106.5g NaClO3为1mol,做氧化剂转化为PdCl42-,转移6mol电子,即1g NaClO3参与反应得到![]() mol≈0.056mol电子,两者相比,NaClO3的氧化效率更高。
mol≈0.056mol电子,两者相比,NaClO3的氧化效率更高。
(5)“沉淀”时,[Pd(NH3)4]2+转化为[Pd(NH3)2]Cl2沉淀,其化学方程式为[Pd(NH3)4]Cl2+2HCl=[Pd(NH3)2]Cl2↓+2NH4Cl;
(6) ①BrO3-能在负载Pd/A12O3纳米催化剂的电极表面快速转化为Br-,溴元素的化合价降低,得电子,发生还原反应,负载Pd/A12O3纳米催化剂的电极作阴极,电解池的阴极与电源的负极相连;
②电流密度越大,电催化效率越高;酸性条件下,但当电流密度过大时,进入到阴极的电子过多,多余的电子来不及被BrO3-得到转化为Br-,电解质溶液中的氢离子会结合多余的电子,则出现电极副反应:H++2e-=H2↑。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案