题目内容
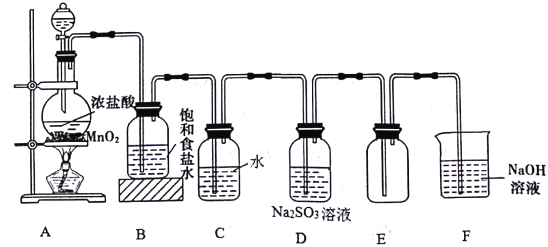
【题目】化学探究学习小组的同学用下图所示装置制取氯气并探究氯气的某些性质。
(1)装置A中制取Cl2的化学方程式为________________________。
(2)装置C中发生反应的离子方程式为_________________,反应后溶液中含Cl元素的分子有_________。
(3)实验结束后,测得装置D溶液中存在大量SO42-。Cl2通过装置D溶液时发生反应的离子方程式为 _____________ 。
(4)装置F的作用是______,该装置中发生反应的离子方程式______________。
【答案】 MnO2 +4HCl(浓)![]() MnCl2+Cl2↑+2H2O Cl2+ H2O =H++Cl- +HClO Cl2、HC1O Cl2+ H2O + SO32-= SO42 -+Cl-+ 2H+ 吸收多余的Cl2,防止环境污染 Cl2 +2OH-= H2O +Cl + ClO-
MnCl2+Cl2↑+2H2O Cl2+ H2O =H++Cl- +HClO Cl2、HC1O Cl2+ H2O + SO32-= SO42 -+Cl-+ 2H+ 吸收多余的Cl2,防止环境污染 Cl2 +2OH-= H2O +Cl + ClO-
【解析】装置A是氯气发生装置,生成的氯气含水蒸气和氯化氢气体,通过装置B中饱和食盐水除去氯化氢,通过装置C吸收氯气形成氯水,通过装置D中亚硫酸钠和氯气反应氧化还原反应生成硫酸钠,E装置是收集氯气,F装置是吸收剩余氯气。
(1)装罝A中制取Cl2的化学方程式为MnO2 +4HCl(浓)![]() MnCl2+C12↑+2H2O;(2)氯气和水反应生成氯化氢和次氯酸,次氯酸为弱酸,装罝C中发生反应的离子方程式为:Cl2+H2O═H++Cl-+HClO,反应后溶液中含有的具有氧化性的含Cl元素的分子有 Cl2、HClO;(3)氯气将亚硫酸根离子氧化成硫酸根离子,氯气被还原为氯离子,Cl2通过装置D溶液时发生反应的离子方程式为:Cl2+H2O+SO32-═SO42-+2Cl-+2H+;(4)氯气有毒,装置F的作用是吸收多余的Cl2,防止环境污染,反应的离子方程式为:Cl2+2OH-═H2O+Cl-+ClO-。
MnCl2+C12↑+2H2O;(2)氯气和水反应生成氯化氢和次氯酸,次氯酸为弱酸,装罝C中发生反应的离子方程式为:Cl2+H2O═H++Cl-+HClO,反应后溶液中含有的具有氧化性的含Cl元素的分子有 Cl2、HClO;(3)氯气将亚硫酸根离子氧化成硫酸根离子,氯气被还原为氯离子,Cl2通过装置D溶液时发生反应的离子方程式为:Cl2+H2O+SO32-═SO42-+2Cl-+2H+;(4)氯气有毒,装置F的作用是吸收多余的Cl2,防止环境污染,反应的离子方程式为:Cl2+2OH-═H2O+Cl-+ClO-。

【题目】在呼吸面具和潜水艇中可用过氧化钠作为供养剂。请选择适当的化学试剂和实验 用品,用下图中的实验装置进行试验,证明过氧化钠可作供养剂。

(1)A是制取CO2的装置。写出A中发生反应的化学方程式:__________________。
(2)填写表中空格:
仪器 | 加入试剂 | 加入试剂的目的 |
B | 饱和NaHCO3溶液 | ____________ |
C | _________________ | ____________ |
D | _________________ | ____________ |


