题目内容
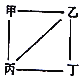
【题目】X、Y、Z、W为原子序数递增的4种短周期元素,其中Y、Z为金属元素。X、Y、Z、W的最高价氧化物对应的水化物甲、乙、丙、丁之间存在如图所示反应关系(图中“一”相连的两种物质能发生反应)。下列判断一定正确的是( )
A. X是元素周期表中非金属性最强的元素 B. Z位于元素周期表第3周期ⅠA族
C. 4种原子中,Y原子半径最大 D. W的最高化合价为+7
【答案】C
【解析】Y、Z为金属元素,由转化关系可知对应的最高价氧化物对应的水化物可发生反应,由原子序数关系可知Y为Na、Z为Al,则乙为NaOH,丙为Al(OH)3,甲、丁应为含氧酸,由原子序数关系可知X为N元素,甲为HNO3,W可能为S、Cl等元素,丁可为硫酸、高氯酸,由以上分析可知X为N、Y为Na、Z为Al、W可能为S、Cl等元素,则A.X为N元素,如为非金属性最强的元素,应为F,则无正价,A错误;B.Z为Al、位于周期表第三周期ⅢA族,B错误;C.Y为Na,为短周期半径最大的元素,C正确;D.如W为S,则最高化合价为+6价,D错误,答案选C。
电解:本题考查无机物的推断,侧重考查学生的分析能力,注意把握物质的性质以及转化关系,本题突破口为乙、丙的反应,另外需要注意F元素没有正价,氧元素没有最高价。

练习册系列答案
相关题目