��Ŀ����
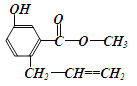
����Ŀ��I��д�����л���������ƻ�ṹ��ʽ��
��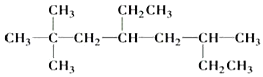 ������Ϊ________________________.
������Ϊ________________________.
��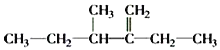 ������Ϊ______________________________.
������Ϊ______________________________.
II����֪�л�������X�и�Ԫ�ص����������ֱ�ΪC---60%��H---13.3%��O---26.7%��
����գ�
��1���л���X��ʵ��ʽΪ____________����0.1molX�����������г��ȼ������������10.08L����״��������X�ķ���ʽΪ________��
��2��ʵ�������X��������Ʒ�Ӧ����H2��X���ӵĺ˴Ź�����������4�����շ壬�����֮��Ϊ3:2:2:1����X�����к��еĹ����ŵ�����Ϊ_________��X�Ľṹ��ʽΪ_____________��
��3��X������ͬ���칹��Y��Z������Y��������Ʒ�Ӧ����H2����Z���ܡ���Y��Z�Ľṹ��ʽ�ֱ�Ϊ_______________��_______________
���𰸡� 2��2��6��������4-�һ����� 3������2���һ���1����ϩ C3H8O C3H8O �ǻ� ![]()
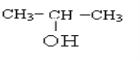
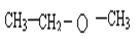
��������I����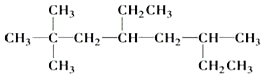 ���̼������8��Cԭ�ӣ�����֧���Ͻ�����˿�ʼ��ţ�2��C����2������6��C��Ҳ��1������4��C����1���һ���������ϵͳ������������Ϊ2��2��6��������4-�һ����� .
���̼������8��Cԭ�ӣ�����֧���Ͻ�����˿�ʼ��ţ�2��C����2������6��C��Ҳ��1������4��C����1���һ���������ϵͳ������������Ϊ2��2��6��������4-�һ����� .
��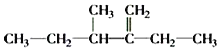 �İ���������̼̼˫�����ڵ��̼������5��Cԭ�ӣ���������ŽϽ���̼ԭ�ӿ�ʼ��ţ�2��Cԭ������1���һ���3��Cԭ������1����������������Ϊ3������2���һ���1����ϩ.
�İ���������̼̼˫�����ڵ��̼������5��Cԭ�ӣ���������ŽϽ���̼ԭ�ӿ�ʼ��ţ�2��Cԭ������1���һ���3��Cԭ������1����������������Ϊ3������2���һ���1����ϩ.
II����X�и�Ԫ�ص����������ֱ�ΪC---60%��H---13.3%��O---26.7%���������C��H��OԪ�ص�ԭ�Ӹ�����Ϊ![]() ��
�� ![]() ��
�� ![]() =3��8��1.
=3��8��1.
��1���л���X��ʵ��ʽΪC3H8O����0.1molX�����������г��ȼ�������ı�״������10.08L��0.45mol������1molX����������4.5mol����X�ķ���ʽΪC3H8O��������ʵ��ʽ��Hԭ�����Ѵﱥ��Ҳ��ȷ������ʽ�ˡ���
��2��X��������Ʒ�Ӧ����H2������Xһ���Ǵ���X���ӵĺ˴Ź�����������4�����շ壬�����֮��Ϊ3:2:2:1����Xһ�����Ҵ���������Ϊ�ǻ����ṹ��ʽΪ![]() ��
��
��3���Ҵ�������ͬ���칹��Y��Z������Y��������Ʒ�Ӧ����H2��Y��2-������Z������Z�Ǽ�������Y��Z�Ľṹ��ʽ�ֱ�Ϊ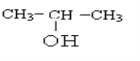 ��
��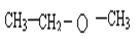 ��
��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ�����к͵ζ����ⶨ�ռ�Ĵ��ȣ����ռ��в��������ᷴӦ�����ʣ��Ը���ʵ��ش�
��1��ȷ��ȡ4.1g�ռ���Ʒ��
��2������Ʒ���250mL����Һ����Ҫ����������С�ձ�������������Ͳ����Ҫ____________________��
��3��ȡ10.00mL����Һ����___________________ ��ȡ��
��4����0.2010mol��L-1������ζ������ռ���Һ��������ָʾ�����ζ�ʱ������ת�ζ��ܵIJ������������ֲ�ͣ��ҡ����ƿ������ע��____________��������______________������ʱ������ζ��յ㡣
��5�������������ݣ���������ռ�Ĵ��ȣ�__________________����������λ��Ч���֣�
�ζ����� | ����Һ��� (mL) | �����������mL�� | |
�ζ�ǰ������mL�� | �ζ��������mL�� | ||
��һ�� | 10.00 | 0.50 | 20.40 |
�ڶ��� | 10.00 | 0.10 | 22.10 |
������ | 10.00 | 4.00 | 24.10 |
��6�����²�������ɲ������ƫ�ߵ�����_________��
��������ˮ��ϴ��ƿ��
���ڵζ������в�����������Һ������ƿ�⣻
�۶���ʱ���ζ�ǰ���ӣ��ζ����ӣ�
��װ��Һ֮ǰ��û���ñ�Һ��ϴ�ζ���;
����Ŀ������һƿA��B�Ļ�����֪���ǵ��������±���
���� | �۵�/�� | �е�/�� | �ܶ�/g��cm��3 | �ܽ��� |
A | ��11.5 | 198 | 1.11 | A��B���ܣ��Ҿ�������ˮ |
B | 17.9 | 290 | 1.26 |
�ݴ˷�������A��B�����ij��÷�����
A. ���� B. ���� C. ��Һ D. ����