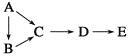题目内容
【题目】Mn2+催化H2O2分解:2H2O2(aq)===2H2O(l)+O2(g) ΔH1,其反应机理如下:
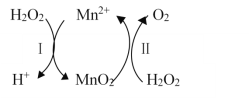
若反应Ⅱ的晗变为ΔH2,反应Ⅰ、Ⅱ的化学计量数均为最简整数比,则反应Ⅰ的晗变ΔH为( )
A. ΔH1+ΔH2 B. ΔH1-ΔH2 C. 2ΔH1-ΔH2 D. ΔH1-2ΔH2
【答案】B
【解析】
根据化学反应的焓变只与反应体系的始态(各反应物)和终态(各反应物)有关系,而与反应途径无关即盖斯定律来解题即可。
Mn2+催化H2O2分解:2H2O2(aq)=2H2O(l)+O2(g) ΔH1①
反应Ⅱ为MnO2(s)+ H2O2(aq)+2H+(aq)= Mn2+(aq)+O2(g) + 2H2O(l) ΔH2 ②
反应Ⅰ为Mn2+(aq)+H2O2(aq)=2H+(aq)+MnO2(s) ΔH
①-②可得反应Ⅰ,因此ΔH=ΔH1-ΔH2,即选项B正确。

【题目】丙酮的碘代反应![]() 的速率方程为
的速率方程为![]() ,其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为
,其半衰期(当剩余反应物恰好是起始的一半时所需的时间)为![]() 改变反应物浓度时,反应的瞬时速率如表所示。
改变反应物浓度时,反应的瞬时速率如表所示。
|
|
|
0.25 | 0.050 | 1.4 |
0.50 | 0.050 | 2.8 |
1.00 | 0.050 | 5.6 |
0.50 | 0.100 | 2.8 |
下列说法正确的是( )
A.速率方程中的![]() 、
、![]()
B.该反应的速率常数![]()
C.增大![]() 的浓度,反应的瞬时速率加快
的浓度,反应的瞬时速率加快
D.在过量的![]() 存在时,反应掉87.5%的
存在时,反应掉87.5%的![]() 所需的时间是375min
所需的时间是375min
【题目】下表各物质中,A、B、C、D、E均含有同一种短周期元素,其中A是单质,B常温下是气态氢化物,C、D是氧化物,E是D和水反应的产物。则各物质之间通过一步反应就能实现表中所示转化的是 ( )
物质编号 | 物质转化关系 | A | D | E |
① |
| Si | SiO2 | Na2SiO3 |
② | S | SO3 | H2SO4 | |
③ | Na | Na2O2 | NaOH | |
④ | N2 | NO2 | HNO3 |
A.②③ B.②④ C.①③④ D.①②③④