题目内容
【题目】某温度时,在容积为2 L的密闭容器中,A、B、C三种气态物质的物质的量随时间变化的曲线如图所示。
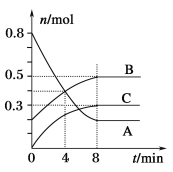
分析图中数据,回答下列问题:
(1)该反应的化学方程式为______________。
(2)反应开始至4 min时,物质A的平均反应速率为____。
(3)4 min时,正反应速率_______(填“>”“<”或“=”,下同)逆反应速率,8 min时,正反应速率________逆反应速率。
【答案】2A(g) B(g) +C(g) 0.15mol/(Lmin) > =
【解析】
(1)由图可知,8min末达到平衡状态,说明该反应为可逆反应,从反应开始到8min末,A的物质的量减少0.6mol、B的物质的量增加0.3mol,C的物质的量增加0.3mol,
因此该反应的化学方程式为2A(g) B(g) +C(g);
(2)反应开始至4min末,A的物质的量减少了0.6mol,v(A)=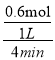 =0.15mol/(Lmin);
=0.15mol/(Lmin);
(3)4min的时候反应物的浓度仍然再继续减少,所以反应向正反应方向进行,即v(正)>v(逆)。8 min时,物质的浓度不再发生变化,反应达到平衡状态,所以v(正)=v(逆)。

练习册系列答案
相关题目