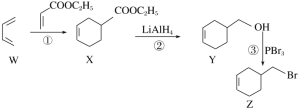
题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法错误的是( )
A.1 mol![]() OD- 离子含有的质子、中子数均为9NA
OD- 离子含有的质子、中子数均为9NA
B.3.6 g石墨和C60的混合物中,含有的碳原子数为0.3NA
C.含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA
D.标准状况下,4.48 L戊烷含有的分子数为0.2NA
【答案】D
【解析】
A选项,1个![]() OD-含有9个质子,9个中子,因此1 mol
OD-含有9个质子,9个中子,因此1 mol![]() OD-离子含有的质子、中子数均为9NA,故A正确;
OD-离子含有的质子、中子数均为9NA,故A正确;
B选项,石墨和C60都是由碳组成的,可以用通式Cn来描述,即3.6g石墨和C60的混合物物质的量为![]() ,含有的碳物质的量为0.3mol,则碳原子数为0.3NA,故B正确;
,含有的碳物质的量为0.3mol,则碳原子数为0.3NA,故B正确;
C选项,含有4.6 g钠元素即钠的物质的量为0.2mol,其过氧化钠和氧化钠的混合物为0.1mol,无论过氧化钠还是氧化钠,1mol都含有3mol离子,因此0.1mol混合物所含离子总数为0.3NA,故C正确;
D选项,标准状况下,戊烷是液体,不能用气体摩尔体积进行计算,故D错误。
综上所述,答案为D。

【题目】科学家一直致力于“人工固氮”的方法研究。
(1)合成氨的原理为:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)![]() H=-92.4 kJ/mol,该反应的能量变化如图所示。
H=-92.4 kJ/mol,该反应的能量变化如图所示。
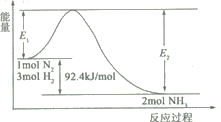
①在反应体系中加入催化剂,反应速率增大,E2的变化是___(填“增大”、“减小”或“不变”)。
②将0.3 mol N2和0.5 mol H2充入体积不变的密闭容器中,在一定条件下达到平衡,测得容器内气体压强变为原来的![]() ,此时H2的转化率为___;欲提高该容器中H2的转化率,下列措施可行的是___(填选项字母)。
,此时H2的转化率为___;欲提高该容器中H2的转化率,下列措施可行的是___(填选项字母)。
A.向容器中按原比例再充入原料气 | B.向容器中再充入一定量H2 |
C.改变反应的催化剂 | D.液化生成物分离出氨 |
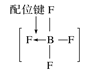
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生反应:
2N2(g)+6H2O(1)![]() 4NH3(g)+3O2(g)
4NH3(g)+3O2(g)![]() H=+1530 kJ/mol
H=+1530 kJ/mol
又知:H2O(1)=H2O(g)![]() H=+44.0 kJ/mol
H=+44.0 kJ/mol
则2N2(g)+6H20(g)![]() 4NH3(g)+302(g)
4NH3(g)+302(g)![]() H =___kJ/mol,该反应的化学平衡常数表达式为K=_______,控制其他条件不变,增大压强,K值___(填“增大”、“减小”或“不变”)。
H =___kJ/mol,该反应的化学平衡常数表达式为K=_______,控制其他条件不变,增大压强,K值___(填“增大”、“减小”或“不变”)。