题目内容
6.选择下列实验方法分离物质,将分离方法的序号填在横线上.A.萃取分液 B.升华 C.结晶 D.过滤 E.蒸馏 F.分液
(1)分离饱和食盐水与沙子的混合物D
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾C
(3)从碘水中提取碘单质A
(4)分离氯化钠固体和碘单质的混合物B
(5)分离水和汽油的混合物F
(6)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物E.
分析 (1)沙子不溶于水;
(2)硝酸钾和氯化钠的溶解度受温度影响不同;
(3)碘不易溶于水,易溶于有机溶剂;
(4)碘易升华,而氯化钠不能;
(5)水和汽油分层;
(6)CCl4和甲苯互溶,但沸点不同.
解答 解:(1)沙子不溶于水,则选择过滤法分离,故答案为:D;
(2)硝酸钾和氯化钠的溶解度受温度影响不同,则选择结晶法分离出硝酸钾,故答案为:C;
(3)碘不易溶于水,易溶于有机溶剂,则利用有机溶剂萃取碘水中的碘,分液可分离,故答案为:A;
(4)碘易升华,而氯化钠不能,则升华法可分离,故答案为:B;
(5)水和汽油分层,则选择分液法分离,故答案为:F;
(6)CCl4和甲苯互溶,但沸点不同,则选择蒸馏法分离,故答案为:E.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异、混合物分离方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
14.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水反应的化学方程式是:4K2FeO4+10H2O═4Fe(OH)3(胶体)+3O2↑+8KOH工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入一定量的KOH就可制得高铁酸钾.制备高铁酸钠的两种方法的主要反应原理如下:
湿法制备:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O
干法制备:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法中错误的是( )
湿法制备:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3NaCl+5H2O
干法制备:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列有关说法中错误的是( )
| A. | 高铁酸钾处理水时,水发生氧化反应 | |
| B. | 湿法中每生成1mol Na2FeO4共转移3mol电子 | |
| C. | 干法中每生成1mol Na2FeO4共转移3mol电子 | |
| D. | K2FeO4处理水时,不仅能杀菌,并能使悬浮杂质沉降 |
1.下列溶液中的c (Cl-)与50mL 1mol•L-1氯化铝溶液中的c (Cl-)相等的是( )
| A. | 150mL 1mol•L-1氯化钠溶液 | B. | 159mL 3mol•L-1氯化钾溶液 | ||
| C. | 75mL 1mol•L-1氯化镁溶液 | D. | 75mL 2mol•L-1氯化钙溶液 |
11.已知氮化铝的晶胞结构如图所示,下列说法正确的是( )


| A. | 氮化铝晶胞结构与NaCl相同 | B. | 第一电离能N<Al | ||
| C. | 电负性N>Al | D. | 原子半径N>Al |
18.下列不是海水淡化主要方法的是( )
| A. | 蒸馏法 | B. | 离子交换法 | C. | 电渗析法 | D. | 干馏法 |
15.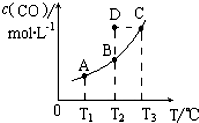 在恒容密闭容器中存在下列平衡:C(s)+H2O(g)?CO(g)+H2(g)的平衡物质的量浓度与温度 T的关系如图所示.下列说法错误的是( )
在恒容密闭容器中存在下列平衡:C(s)+H2O(g)?CO(g)+H2(g)的平衡物质的量浓度与温度 T的关系如图所示.下列说法错误的是( )
 在恒容密闭容器中存在下列平衡:C(s)+H2O(g)?CO(g)+H2(g)的平衡物质的量浓度与温度 T的关系如图所示.下列说法错误的是( )
在恒容密闭容器中存在下列平衡:C(s)+H2O(g)?CO(g)+H2(g)的平衡物质的量浓度与温度 T的关系如图所示.下列说法错误的是( )| A. | 该反应的△H>0 | |
| B. | 若T1、T2 时的平衡常数分别为K1、K2,则K1=K2 | |
| C. | 通过加热可以使B 点变到C 点 | |
| D. | 在T2时若反应进行到状态D,则一定有υ(正)<υ(逆) |
 ,A既能与强酸又能与强碱反应,且都能产生气体,则A的化学式为(NH4)2S或NH4HS.
,A既能与强酸又能与强碱反应,且都能产生气体,则A的化学式为(NH4)2S或NH4HS.