题目内容
18.在下列几种物质中跟HCl溶液和NaOH溶液都能发生反应的是( )①NaHCO3、②Al(OH)3、③(NH4)2CO3、④SiO2、⑤金属铝、⑥A12O3.
| A. | 只有②④⑥ | B. | 只有①⑤⑥ | C. | 只有①②③⑤⑥ | D. | 全部都可以 |
分析 Al、Al2O3、Al(OH)3、弱酸的酸式盐、弱酸对应的铵盐、蛋白质、氨基酸等既能跟NaOH溶液反应,又能跟盐酸反应.
解答 解:碳酸氢钠是弱酸酸式盐,能和盐酸、氢氧化钠反应,故选;
氢氧化铝是两性氢氧化物,能和盐酸、氢氧化钠反应生成盐和水,故选;
碳酸铵是弱酸的铵盐,能和盐酸、氢氧化钠反应,故选;
二氧化硅是酸性氧化物,只能和氢氧化钠反应,但不能和稀盐酸反应,故不选;
Al性质具有两性,能和稀盐酸、氢氧化钠反应生成盐和氢气,故选;
氧化铝是两性氧化铝,能和稀盐酸、氢氧化钠反应生成盐和水,故选;
故选C.
点评 本题考查元素化合物知识,明确物质性质是解本题关键,注意总结归纳具有两性的物质,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 60g丙醇存在的共价键总数为10 NA | |
| B. | 常温常压下,28 g C2H4和CO的混合气体中含有碳原子的数目为1.5NA | |
| C. | 7.2g新戊烷与异戊烷的混合物中所含极性共价键的数目为1.2NA | |
| D. | 标准状况下,11.2 L乙醇中含有的碳氢键数为2.5NA |
9.下列化学用语正确的是( )
| A. | CH4分子的比例模型: | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 甲醛分子的电子式: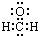 | D. | 基态硫原子的价电子排布:2s22p4 |
6.在一定温度下的恒容密闭容器中,能说明反应X2(g)+Y2(g)?$?_{△}^{浓硫酸}$?2XY(g)已达到平衡的是( )
| A. | 容器内的总压不随时间变化 | |
| B. | 容器中气体的平均相对分子质量不随时间变化 | |
| C. | XY气体的物质的量分数不变 | |
| D. | X2和Y2的消耗速率相等 |
10.下列说法正确的是( )
| A. | HF比HCl稳定是由于HF分子间存在氢键所引起的 | |
| B. | 水在结冰时密度变小是由于水分子间存在氢键所引起的 | |
| C. | CH4分子很稳定,是由于分子间氢键的存在而导致的 | |
| D. | 离子化合物肯定含有金属元素,故在微粒间不存在共价键 |
7.下列有关实验操作和说法中,正确的是( )
| A. | 乙烷中混有乙烯,通过盛有酸性KMnO4溶液的洗气瓶洗气除去乙烯 | |
| B. | 检验C2H5Cl中氯原子时,将C2H5Cl和NaOH溶液混合加热后,加入稀硫酸酸化 | |
| C. | 用无水乙醇和浓H2SO4共热至140℃可以制得乙烯气体 | |
| D. | 制取溴苯应用液溴、铁屑和苯混合,反应后并用稀碱液洗涤 |




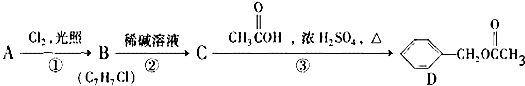
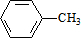 ,C的名称:苯甲醇.
,C的名称:苯甲醇. +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$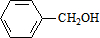 +NaCl.
+NaCl. .
. .
.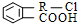 (其中R为饱和烃基),在一定条件下发生如图所示转化关系:
(其中R为饱和烃基),在一定条件下发生如图所示转化关系: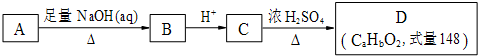
 或
或 .
. .
.