题目内容
【题目】如图所示a、b都是惰性电极,通电一段时间后,a极附近溶液显红色。下列说法中正确的是( )
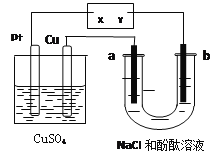
A. X是正极,Y是负极 B. U型管中溶液PH值逐渐变小
C. CuSO4溶液的pH逐渐减小 D. CuSO4溶液的pH保持不变
【答案】C
【解析】
试题A.通电电解氯化钠溶液时,a极附近溶液呈红色,说明a连接电源的负极,则X为负极,Y是正极,A错误;
B.通电电解氯化钠溶液时,总反应为:NaCl+H2O![]() Cl2↑+ H2↑+ 2NaOH ,U型管中溶液PH值逐渐变大,B错误;
Cl2↑+ H2↑+ 2NaOH ,U型管中溶液PH值逐渐变大,B错误;
C.电解硫酸铜时,总反应为:2CuSO4+2H2O![]() 2Cu+2H2SO4+O2↑根据电解方程式可确定溶液pH逐渐减小,C正确;
2Cu+2H2SO4+O2↑根据电解方程式可确定溶液pH逐渐减小,C正确;
D.根据电解方程式可确定溶液pH逐渐减小,D错误。故选C。

【题目】I. 已知:
反应Fe(s)+CO2(g)![]() FeO(s)+CO(g)的平衡常数为K1;
FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)![]() FeO(s)+H2(g)的平衡常数为K2。
FeO(s)+H2(g)的平衡常数为K2。
在不同温度时K1、K2的值如下表:
温度(绝对温度) | K1 | K2 |
973 | 1.47 | 2.38 |
1173 | 2.15 | 1.67 |
(1)推导反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:___________,判断该反应是___________反应(填“吸热”或“放热”)。
CO(g)+H2O(g)的平衡常数K与K1、K2的关系式:___________,判断该反应是___________反应(填“吸热”或“放热”)。
II. T1温度下,体积为 2L的恒容密闭容器,加入4.00molX,2.00molY,发生化学反应 2X(g)+Y(g)![]() 3M(g)+N(s) △H<0。部分实验数据如表格所示。
3M(g)+N(s) △H<0。部分实验数据如表格所示。
t/s | 0 | 500 | 1000 | 1500 |
n(X)/mol | 4.00 | 2.80 | 2.00 | 2.00 |
(2)前500s反应速率v(M)=____________,该反应的平衡常数K=_____________。
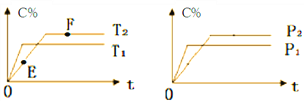
(3)该反应达到平衡时某物理量随温度变化如下图所示。纵坐标可以表示的物理量有哪些_____。

a.Y的逆反应速率 b.M的体积分数
c.混合气体的平均相对分子质量 d.X的质量分数
(4)反应达到平衡后,若再加入3.00molM,3.00molN,下列说法正确的是_____。
A.平衡不移动
B.重新达平衡后,M的体积分数小于50%
C.重新达平衡后,M的物质的量浓度是原平衡的1.5倍
D.重新达平衡后,Y的平均反应速率与原平衡相等
E.重新达平衡后,用X表示的v(正)比原平衡大
(5)若容器为绝热恒容容器,起始时加入4.00molX,2.00molY,则达平衡后M的物质的量浓度_____1.5mol/L(填“>”、“=”或“<”)。