题目内容
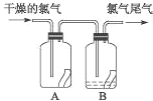
【题目】(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是:__________
(2)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用_________溶液吸收多余的氯气,原理是(用化学方程式表示)_________________
(3)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,反应的化学方程式是__________
【答案】干燥的有色布条不褪色,湿润的有色布条褪色 NaOH溶液 Cl2+2NaOH=NaCl+NaClO+H2O 2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
【解析】
(1)氯气没有漂白性,氯气和水反应生成的HClO有漂白性,所以将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到干燥的有色布条不褪色,湿润的有色布条褪色。
(2)氯气有毒,是大气污染物,为了防止氯气污染空气,需要进行尾气处理。氯气和NaOH溶液可以发生比较完全而快速的反应,所以用NaOH溶液吸收多余的氯气。反应的化学方程式为:Cl2+2NaOH=NaCl+NaClO+H2O。
(3)氯气和石灰乳的反应和氯气和NaOH的反应原理相同,都是歧化反应,生成金属氯化物、次氯酸盐和水,反应的化学方程式为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。

练习册系列答案
相关题目