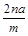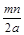题目内容
下列4种装置工作一段时间后,测得导线上均通过了0.002 mol 电子,此时溶液的pH值由大到小的排列顺序为(不考虑盐的水解和溶液体积变化)①盛100 mL CuSO4 ②盛200 mL 0.01 mol·L-1 H2SO4 ③盛200 mL ZnCl2 ④盛200 mL NaCl饱和溶液( )


| A.④②③① | B.④③②① | C.④③①② | D.④①③② |
C
考查电化学的有关判断及计算。装置①中锌是阳极,失去电子,铜离子在阴极得到电子,所以pH不变;装置②中,阳极是惰性电极,相当于电解水,硫酸的浓度增大,pH降低;装置③是铁上镀锌,溶液的pH不变;装置④中阳极是惰性电极,反应中生成氯气、氢气和氢氧化钠,溶液的pH增大,所以正确的答案选C。

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目