题目内容
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 标准状况下,2.24LSO3中含有0.1NA个SO3分子
B. 向1L的密闭容器中充入46gNO2气体,容器中气体的分子数为NA
C. 常温下,将2.7g铝片投入足量的浓硫酸中,转移电子的数目为0.3NA
D. ![]() 的同分异构体中含有苯环且属于羧酸的有14种
的同分异构体中含有苯环且属于羧酸的有14种
【答案】D
【解析】A. 根据标准状况下,SO3不是气体分析;B. 根据NO2中存在平衡:2NO2N2O4分析;C. 根据常温下,铝与浓硫酸发生钝化分析;D. ![]() 的同分异构体中含有苯环且属于羧酸的结构中一定含有羧基、苯环,其余2个碳原子分情况书写分析判断。
的同分异构体中含有苯环且属于羧酸的结构中一定含有羧基、苯环,其余2个碳原子分情况书写分析判断。
A. 标准状况下,SO3不是气体,无法用n=![]() 计算2.24LSO3的物质的量,故A错误;B、NO2中存在平衡:2NO2N2O4,导致分子个数减小,则容器中气体分子个数小于NA个,故B错误;C. 常温下,铝与浓硫酸发生钝化,2.7g铝不能完全反应,故C错误;D.
计算2.24LSO3的物质的量,故A错误;B、NO2中存在平衡:2NO2N2O4,导致分子个数减小,则容器中气体分子个数小于NA个,故B错误;C. 常温下,铝与浓硫酸发生钝化,2.7g铝不能完全反应,故C错误;D.![]() 的同分异构体中含有苯环且属于羧酸的有:①羧基直接与苯环连接,剩余两个碳作为乙基存在邻、间、对3种同分异构体,作为两个甲基存在6种同分异构体;②骨架为苯乙酸,甲基存在邻、间、对3种同分异构体;③苯丙酸有2种,共14种同分异构体,故D正确;故选D。
的同分异构体中含有苯环且属于羧酸的有:①羧基直接与苯环连接,剩余两个碳作为乙基存在邻、间、对3种同分异构体,作为两个甲基存在6种同分异构体;②骨架为苯乙酸,甲基存在邻、间、对3种同分异构体;③苯丙酸有2种,共14种同分异构体,故D正确;故选D。

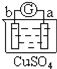
【题目】X、Y、Z三种物质存在如图所示的转化关系(图中“→”表示一步转化)。下列各组物质中,不能满足此转化关系的是( )
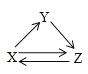
物质 选项 | X | Y | Z |
A | Al | Al2O3 | NaAlO2 |
B | Fe | FeCl3 | FeCl2 |
C | C | CO | CO2 |
D | Cl2 | HCl | NaCl |
A. A B. B C. C D. D
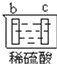
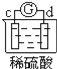
【题目】有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
实验装置 |
|
|
|
|
部分实验现象 | a极质量减小 b极质量增加 | b极有气体产生 c极无变化 | d极溶解 c极有气体产生 | 电流计指示在导线中 电流从a极流向d极 |
由此可判断这四种金属的活动性顺序是( )
A. d>a>c>bB. b>c>d>aC. d>a>b>cD. a>b>d>c