题目内容
下列关于溶液中的描述正确的是
A.常温时, 溶液的 溶液的 ,则该溶液中 ,则该溶液中 |
B. 溶液与 溶液与 溶液反应至中性的离子方程式为: 溶液反应至中性的离子方程式为: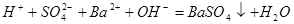 |
C.常温下物质的量浓度相等的下列四种溶液:① ;② ;② ;③ ;③ ;④ ;④ ,四种溶液中 ,四种溶液中 比较:② 比较:② ① ① ④ ④ ③ ③ |
D.常温下 的溶液: 的溶液: 、 、 、 、 、 、 可以常量共存 可以常量共存 |
A
A中根据电荷守恒c(H+)+c(Na+)=c(NO2-)+c(OH-)可知,c(Na+)-c(NO2-)=c(OH-)-c(H+)=10-6mol/L-10-8mol/L=9.9×10-7mol/L,A正确。B不正确,应该是2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O。硫酸氢铵能电离出氢离子,抑制NH4+水解。同样亚铁离子水解也显酸性,抑制NH4+水解。醋酸铵中CH3COO-水解显碱性,促进NH4+水解,溶液中NH4+浓度从大到小的顺序是①④③②,C不正确。选项D中氢离子浓度是10-4mol/L,即溶液显酸性,能产生硅酸沉淀,D不正确,答案选A。

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目