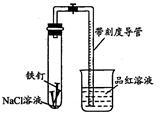
��Ŀ����
Ϊ֤����ѧ��Ӧ��һ�����ȣ���������̽�����
I��ȡ5mL 0.1mol/L��KI��Һ���μ�5��6��FeCl3ϡ��Һ��
��������2mL CCl4���Ǻò����������á�
��ȡ������Һ��õ����ϲ���Һ���μ�KSCN��Һ��
������ȡ25.00mLFeCl3ϡ��Һ����ƿ�У�����KSCN��Һ����ָʾ��������c mol/LKI����Һ�ζ����ﵽ�ζ��յ㡣�ظ��ζ����Σ�ƽ������c mol/LKI����ҺVmL��
��1��̽���I�з�����Ӧ�����ӷ���ʽΪ ��
�뽫̽������С����á���õ��²�Һ��IJ�����������������Һ©����������̨�ϣ����á�
��
��2��̽��������ͼ��ͨ�����ɺ�ɫ����Һ����������ȫ��ΪFe(SCN)3������֤��Fe3+�������Ӷ�֤����ѧ��Ӧ��һ�����ȣ�����ʵ����ȴδ����Һ�ʺ�ɫ���Դ�ͬѧ��������������ֲ��룺
����һ��Fe3+ȫ��ת��ΪFe2+ ����������ɵ�Fe(SCN)3Ũ�ȼ�С������ɫ�������۲졣
Ϊ����֤���룬�������ϻ��������Ϣ��
��Ϣһ����������ˮ���ܶ�Ϊ0.71g/mL��Fe(SCN)3�������е��ܽ�ȱ���ˮ�д�
��Ϣ����Fe3+����[Fe(CN)6]4����Ӧ���ɰ���ɫ��������K4[Fe(CN)6](�����軯��)��Һ����Fe3+�������ȱ���KSCN��Һ���ߡ�
�������Ϣ�����������ʵ�鷽����֤���룺
��������±�
| ʵ����� | ����ͽ��� |
| ����һ�� | ����������ɫ�������� �� |
| ������� | �����Ѳ�ʺ�ɫ���� �� |
��д��ʵ�����������һ���еķ�Ӧ���ӷ���ʽ�� ��
��3������̽�������FeCl3ϡ��Һ���ʵ���Ũ��Ϊ mol/L��
����14�֣���1��2Fe3+ + 2I-��2Fe2+ + I2��2�֣�����Һ��ֲ����Һ©�����ϵIJ���������ʹ�������ϵİ��ۣ���С�ף�����Һ©���ϵ�С�ף��ٽ���Һ©������Ļ���š����ʹ�²�Һ���������ձ������¡���2�֣�
��2��ʵ����� ����ͽ��� ����һ��ȡ��ȡ��õ����ϲ���Һ������2��K4[Fe(CN)6](�����軯��)��Һ��2�֣� ����������ɫ�����������һ��������1�֣� �������ȡ̽������������Һ�������������ѣ���������÷ֲ㣨2�֣� �����Ѳ�ʺ�ɫ��������������1�֣�
4Fe3+ +3[Fe(CN)6]4����Fe4[Fe(CN)6]3����2�֣� ��3��0.04cV��2�֣�
���������������1�������Ӿ��������ԣ��ܰѵ������������ɵ��ʵ⣬��Ӧ�����ӷ���ʽ��2Fe3+ + 2I-��2Fe2+ + I2��̽������������Ȼ�̼��ȡ���ʵ⣬�����ȷ�IJ����ǽ���Һ©����������̨�ϣ����á���Һ��ֲ����Һ©�����ϵIJ���������ʹ�������ϵİ��ۣ���С�ף�����Һ©���ϵ�С�ף��ٽ���Һ©������Ļ���š����ʹ�²�Һ���������ձ������¡�
��2���ٸ��ݲ���1��ʵ�������Dz�������ɫ��������˵��������Լ���K4[Fe(CN)6](�����軯��)��Һ�����Բ���1��ȡ��ȡ��õ����ϲ���Һ������2��K4[Fe(CN)6](�����軯��)��Һ������������ɫ�����������һ�����������ݲ���2��ʵ�����������Ѳ�ʺ�ɫ����˵��������Լ������ѣ�����2�IJ�����ȡ̽������������Һ�������������ѣ���������÷ֲ㡣�����Ѳ�ʺ�ɫ��������������
�ڸ������Ϸ�����֪��ʵ�����������һ���еķ�Ӧ���ӷ���ʽ��4Fe3+ +3[Fe(CN)6]4����Fe4[Fe(CN)6]3����
��3�����ݷ���ʽ2Fe3+ + 2I����2Fe2+ + I2��֪
Fe3+����������I��
1mol 1mol
0.0250Lx cmol/L��0.001VL
���x��0.04cVmol/L
���㣺����������ԭ��Ӧ����ʽ����д����ȡʵ�������������ѧʵ�鷽������ƣ����ӵļ����Լ�����Ũ�ȵļ����

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�Fenton�������ڴ������ѽ����л���Ĺ�ҵ��ˮ��ͨ�����ڵ��ں�pH��Fe2��Ũ�ȵķ�ˮ�м���H2O2�����������ǻ����ɻ�������������Ⱦ������ø÷��������л���Ⱦ��p��CP��̽���й����ضԸý��ⷴӦ���ʵ�Ӱ�졣
[ʵ�����]������p��CP�ij�ʼŨ����ͬ���㶨ʵ���¶���298 K��313 K(����ʵ���������±�)��������¶Ա�ʵ�顣
(1)���������ʵ����Ʊ�(���в�Ҫ���ո�)��
| ʵ���� | ʵ��Ŀ�� | T/K | pH | c/10��3 mol��L��1 | |
| H2O2 | Fe2�� | ||||
| �� | Ϊ����ʵ�������� | 298 | 3 | 6.0 | 0.30 |
| �� | ̽���¶ȶԽ��ⷴӦ���ʵ�Ӱ�� | | | | |
| �� | | 298 | 10 | 6.0 | 0.30 |
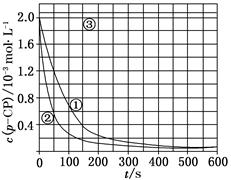
[���ݴ���]��ʵ����p��CP��Ũ����ʱ��仯�Ĺ�ϵ����ͼ��
(2)�������ͼʵ������ߣ����㽵�ⷴӦ50��150 s�ڵķ�Ӧ���ʣ�
v(p��CP)��________mol��L��1��s��1��
[���������]
(3)ʵ��١��ڱ����¶����ߣ����ⷴӦ���������¶ȹ���ʱ�������½��ⷴӦ���ʼ�С�����Fenton�������Լ�H2O2�ĽǶȷ���ԭ��_____________________________
(4)ʵ��۵ó��Ľ����ǣ�pH����10ʱ��________��
[˼���뽻��]
(5)ʵ��ʱ���ڲ�ͬʱ��ӷ�Ӧ����ȡ������ʹ��ȡ��Ʒ�еķ�Ӧ����ֹͣ������������ͼ�е���Ϣ������һ��Ѹ��ֹͣ��Ӧ�ķ�����________��
Ӱ�컯ѧ��Ӧ���ʵ����غܶ࣬ij������ȤС����ʵ��ķ�������̽����
��1��ʵ��һ��ȡ�����ʵ���Ũ�ȵ����H2O2��Һ�ֱ��������ʵ�飬ʵ�鱨�����±���ʾ��
| ��� | ���� | ���� | ���� | |
| �¶�/�� | ���� | |||
| 1 | 40 | FeCl3��Һ | | |
| 2 | 20 | FeCl3��Һ | | |
| 3 | 20 | MnO2 | | |
| 4 | 20 | �� | | |
�Իش�ʵ��1��2�о���������������ͬʱ ��H2O2�ֽ����ʵ�Ӱ�졣
��2��ʵ��������о�֪Cu2����H2O2�ֽ�Ҳ���д����ã�Ϊ�Ƚ�Fe3����Cu2����H2O2�ֽ�Ĵ�Ч������С���ͬѧ�ֱ��������ͼ�ס�����ʾ��ʵ�顣�ش�������⣺
�� ���Է�������ͼ��ͨ���۲�________________________________�����ԱȽϵó����ۡ�
��ͬѧ�����FeCl3��ΪFe2(SO4)3��Ϊ��������������__________________________��
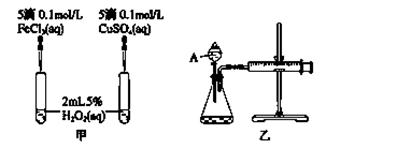
�ڶ���������Ϊ�˸���ȷ���о�Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죬������ͼװ�ý��ж���ʵ�顣��ɸ�ʵ��Ӧ�òⶨ��ʵ��������____________________________________________��
ij��ѧʵ��С���ͬѧ������������װ������ȫ��ͬ��װ�ö���̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�졣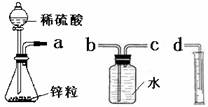
��1��Ϊ�ﵽ��ʵ��Ŀ����װ������˳��Ϊ��a��________��________��________.
��2�����Ӻ�װ�ú����һ��������
��3����ƿ�з�����Ӧ�����ӷ���ʽΪ
��4������װ�õķ�Һ©����װ���Լ��ֱ�Ϊ1mol/L�����4mol/L����,��С��ͬѧҪ�ⶨ����¼���������±���
| ������Լ� | H2���������ͬ�����£� | ��Ӧʱ�� | ��Ӧ���� |
| 1mol/L������ | 10mL | t1 | v1 |
| 4mol/L���� | 10mL | t2 | v2 |
��5������һ��ͬѧ�ⶨ��ÿ��һ���ӣ���ƿ�������Ũ�ȣ���¼������£�

���ڸ���������ͼ������v(H2)-t��ͼ��.
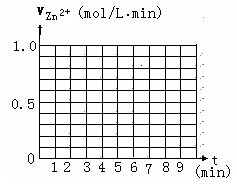
�����0��4mimʱ�û�ѧ��Ӧ������ʱ��仯��ԭ�� .
��6��������ʵ�鷽���ɶ����ⶨ�÷�Ӧ�Ļ�ѧ��Ӧ�����⣬�������е�ʵ��ⶨ�����У� ����дһ�֣�.
�����£���0.1mol/L��̼������Һ�У���������Ũ�ȵĹ�ϵʽ��ȷ����
A��2c(H2CO3)+c(HCO )+c(H+) = c(OH��) )+c(H+) = c(OH��) |
B��c(Na+) = c(HCO )+c(H2CO3)+ 2c(CO )+c(H2CO3)+ 2c(CO ) ) |
C��c(Na+)��c(H+)��c(OH��)��c(CO ) ) |
D��c(Na+)+c(H+) = c(HCO )+c(OH��)+ 2c(CO )+c(OH��)+ 2c(CO ) ) |
���б����У��������ǣ� ��
| A����ˮ���ȣ�Kw���䣬pH���� |
| B����FeCl3��ˮ��Һ�������ɿɵõ�FeCl3���� |
| C����25 mL��ʽ�ζ�����ȡ20.00mL���������Һ |
| D���ö��Ե缫���������AgNO3��Һʱ������0.2 mole-ת��ʱ������21.6g�� |
25��ʱ����0.1mol��L��1��ˮ��Һ��ˮϡ�ͣ�������ֵ������
| A��c(OH��) | B��pH | C��c(NH4+)/c(NH3��H2O) | D��c(H+)��c(OH��) |