题目内容
燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点.下表列出了目前科学家正致力于研究的3种燃煤烟气的脱硫技术和脱硝技术的原理.
(1)方法Ⅰ中有关反应如下:
NO2(g)+SO2(g)+H2O(l)=H2SO4(l)+NO(g)△H1
NO(g)+NO2(g)=N2O3(g)△H2
N2O3(g)+2H2SO4(l)=2NOHSO4(s)+H2O(l)△H3
4NOHSO4(s)+O2(g)+2H2O(l)=4H2SO4(l)+4NO2(g)△H4
2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l)△H5
则△H1、△H2、△H3、△H4、△H5之间的关系为△H5=
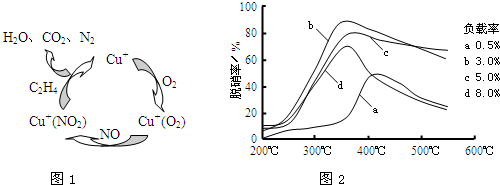
(2)方法Ⅱ的脱硝机理如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.

①出该脱硝过程中乙烯和NO2反应的化学方程式:
②达到最佳脱硝效果,应采取的条件是
(3)方法Ⅲ中用电化学原理将SO2转化为重要的化工原料H2SO4的装置如图(3)所示.
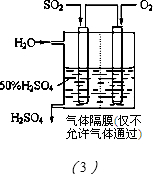
①写出通入SO2的电极的电极反应式:
②为使该脱硫过程稳定持续进行,硫酸溶液的浓度应维持不变,则通入的O2和加入的H2O的质量比为
| 方法Ⅰ | 用硫和氮的氧化物之间的相互转化联合进行的脱硫和脱硝技术 |
| 方法Ⅱ | 用乙烯作为还原剂将氮的氧化物还原为N2的脱硝技术 |
| 方法Ⅲ | 用电化学原理将SO2转化为重要的化工原料H2SO4的脱硫技术 |
NO2(g)+SO2(g)+H2O(l)=H2SO4(l)+NO(g)△H1
NO(g)+NO2(g)=N2O3(g)△H2
N2O3(g)+2H2SO4(l)=2NOHSO4(s)+H2O(l)△H3
4NOHSO4(s)+O2(g)+2H2O(l)=4H2SO4(l)+4NO2(g)△H4
2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l)△H5
则△H1、△H2、△H3、△H4、△H5之间的关系为△H5=
2△H1+2△H2+2△H3+△H4
2△H1+2△H2+2△H3+△H4
.(2)方法Ⅱ的脱硝机理如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.

①出该脱硝过程中乙烯和NO2反应的化学方程式:
2C2H4+6NO2=4CO2+3N2+4H2O
2C2H4+6NO2=4CO2+3N2+4H2O
.②达到最佳脱硝效果,应采取的条件是
350℃(或340℃~360℃)、负载率3%
350℃(或340℃~360℃)、负载率3%
.(3)方法Ⅲ中用电化学原理将SO2转化为重要的化工原料H2SO4的装置如图(3)所示.

①写出通入SO2的电极的电极反应式:
SO2+2H2O-2e-=SO42-+4H+
SO2+2H2O-2e-=SO42-+4H+
.②为使该脱硫过程稳定持续进行,硫酸溶液的浓度应维持不变,则通入的O2和加入的H2O的质量比为
4:29
4:29
.分析:(1)利用盖斯定律计算反应热;
(2)①根据反应物和生成物结合质量守恒定律书写化学方程式;
②根据图象判断最佳脱硝率的温度和负载率;
(3)①通入SO2的电极为原电池的负极,发生氧化反应;
②根据原电池总反应2SO2+2H2O+O2=2H2SO4结合硫酸浓度不变计算.
(2)①根据反应物和生成物结合质量守恒定律书写化学方程式;
②根据图象判断最佳脱硝率的温度和负载率;
(3)①通入SO2的电极为原电池的负极,发生氧化反应;
②根据原电池总反应2SO2+2H2O+O2=2H2SO4结合硫酸浓度不变计算.
解答:解:(1)已知:①NO2(g)+SO2(g)+H2O(l)=H2SO4(l)+NO(g)△H1
②NO(g)+NO2(g)=N2O3(g)△H2
③N2O3(g)+2H2SO4(l)=2NOHSO4(s)+H2O(l)△H3
④4NOHSO4(s)+O2(g)+2H2O(l)=4H2SO4(l)+4NO2(g)△H4
利用盖斯定律将①×2+②×2+③×2+④可得:2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l)
则△H5=2△H1+2△H2+2△H3+△H4,
故答案为:2△H1+2△H2+2△H3+△H4;
(2)①有由图1可知,C2H4和NO2反应生成CO2、N2和H2O,则反应的方程式为2C2H4+6NO2=4CO2+3N2+4H2O,
故答案为:2C2H4+6NO2=4CO2+3N2+4H2O;
②由图2可知,脱硝率最高的曲线为b,此时负载率为3%,最高点为温度为350℃(或340℃~360℃),
故答案为:350℃(或340℃~360℃)、负载率3%;
(3)①通入SO2的电极为原电池的负极,发生氧化反应,生成SO42-,电极反应式为SO2+2H2O-2e-=SO42-+4H+,
故答案为:SO2+2H2O-2e-=SO42-+4H+;
②原电池总反应为2SO2+2H2O+O2=2H2SO4,设通入1molO2,ymol水,则生成2molH2SO4,消耗2mol水,2molSO2,保持硫酸浓度不变,
则有:
×100%=50%,解之得18y=232,
即消耗1molO2,即32g,需要232g水,才能使硫酸浓度不变,则:m(O2):m(H2O)=32:232=4:29,
故答案为:4:29.
②NO(g)+NO2(g)=N2O3(g)△H2
③N2O3(g)+2H2SO4(l)=2NOHSO4(s)+H2O(l)△H3
④4NOHSO4(s)+O2(g)+2H2O(l)=4H2SO4(l)+4NO2(g)△H4
利用盖斯定律将①×2+②×2+③×2+④可得:2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l)
则△H5=2△H1+2△H2+2△H3+△H4,
故答案为:2△H1+2△H2+2△H3+△H4;
(2)①有由图1可知,C2H4和NO2反应生成CO2、N2和H2O,则反应的方程式为2C2H4+6NO2=4CO2+3N2+4H2O,
故答案为:2C2H4+6NO2=4CO2+3N2+4H2O;
②由图2可知,脱硝率最高的曲线为b,此时负载率为3%,最高点为温度为350℃(或340℃~360℃),
故答案为:350℃(或340℃~360℃)、负载率3%;
(3)①通入SO2的电极为原电池的负极,发生氧化反应,生成SO42-,电极反应式为SO2+2H2O-2e-=SO42-+4H+,
故答案为:SO2+2H2O-2e-=SO42-+4H+;
②原电池总反应为2SO2+2H2O+O2=2H2SO4,设通入1molO2,ymol水,则生成2molH2SO4,消耗2mol水,2molSO2,保持硫酸浓度不变,
则有:
| 2mol×98g/mol |
| 2mol×64g/mol+1mol×32g/mol+ymol×18g/mol |
即消耗1molO2,即32g,需要232g水,才能使硫酸浓度不变,则:m(O2):m(H2O)=32:232=4:29,
故答案为:4:29.
点评:本题考查二氧化硫的污染及治理,热化学方程式以及原电池知识,题目综合度较高,难度中等,解答时注意认真分析题给信息,尤其是(3)题,注意从化学方程式的角度解答.

练习册系列答案
相关题目
燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点.下表列出了目前科学家正致力于研究的3种燃煤烟气的脱硫技术和脱硝技术的原理.
| 方法Ⅰ | 用硫和氮的氧化物之间的相互转化联合进行的脱硫和脱硝技术 |
| 方法Ⅱ | 用乙烯作为还原剂将氮的氧化物还原为N2的脱硝技术 |
| 方法Ⅲ | 用电化学原理将SO2转化为重要的化工原料H2SO4的脱硫技术 |
NO2(g)+SO2(g)+H2O(l)=H2SO4(l)+NO(g)△H1
NO(g)+NO2(g)=N2O3(g)△H2
N2O3(g)+2H2SO4(l)=2NOHSO4(s)+H2O(l)△H3
4NOHSO4(s)+O2(g)+2H2O(l)=4H2SO4(l)+4NO2(g)△H4
2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l)△H5
则△H1、△H2、△H3、△H4、△H5之间的关系为△H5=______.
(2)方法Ⅱ的脱硝机理如图1,脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如图2所示.
①出该脱硝过程中乙烯和NO2反应的化学方程式:______.
②达到最佳脱硝效果,应采取的条件是______.
(3)方法Ⅲ中用电化学原理将SO2转化为重要的化工原料H2SO4的装置如图(3)所示.
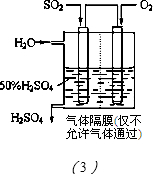
①写出通入SO2的电极的电极反应式:______.
②为使该脱硫过程稳定持续进行,硫酸溶液的浓度应维持不变,则通入的O2和加入的H2O的质量比为______.

 7N2+12H2O
7N2+12H2O  O+O2 Ⅱ、NO+O3→NO2+O2 Ⅲ、NO2+O→NO+O2
O+O2 Ⅱ、NO+O3→NO2+O2 Ⅲ、NO2+O→NO+O2 