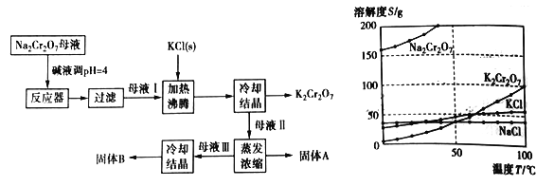
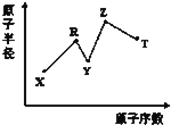
题目内容
【题目】下列各组物质混合反应后,不能生成NaOH的是( )
A.Na和少量CuSO4溶液B.Na2O2和H2OC.Ca(OH)2与Na2CO3 D.Ba(OH)2与NaCl
【答案】D
【解析】
A. Na和少量CuSO4溶液,钠先与水反应生成氢氧化钠和氢气,氢氧化钠与CuSO4溶液反应生成氢氧化铜沉淀,氢氧化钠有剩余,能生成NaOH,故不选A;
B. Na2O2和H2O反应生成氢氧化钠和氧气,能生成NaOH,故不选B;
C. Ca(OH)2与Na2CO3生成碳酸钙沉淀和氢氧化钠,能生成NaOH,故不选C;
D. Ba(OH)2与NaCl不反应,不能生成NaOH,故选D;
故答案选D。

【题目】乙酸乙酯是制药工业和有机合成中的重要原料,实验室制备乙酸乙酯的实验装置![]() 夹持及加热装置已略去
夹持及加热装置已略去![]() 、有关数据和实验步骤如下所示。
、有关数据和实验步骤如下所示。
物质 | 相对分子质量 | 密度 | 沸点 | 在水中的溶解性 |
乙醇 | 46 |
| 80 | 以任意比互溶 |
乙酸 | 60 |
| 118 | 易溶 |
乙酸乙酯 | 88 |
| 77 | 难溶 |
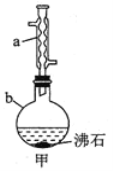
实验步骤:
![]() 向仪器b中加入9.5 mL乙醇(过量)和6 mL乙酸,再缓慢加入2.5 mL浓硫酸,混合均匀后,加入沸石,然后装上冷凝管
向仪器b中加入9.5 mL乙醇(过量)和6 mL乙酸,再缓慢加入2.5 mL浓硫酸,混合均匀后,加入沸石,然后装上冷凝管![]() 如图甲所示
如图甲所示![]() 。
。
![]() 小火加热仪器b,缓慢回流0.5 h,待瓶内反应物冷却后,将回流装置改成蒸馏装置,加热蒸出乙酸乙酯。
小火加热仪器b,缓慢回流0.5 h,待瓶内反应物冷却后,将回流装置改成蒸馏装置,加热蒸出乙酸乙酯。
![]() 向馏出液中缓慢加入5mL饱和碳酸钠溶液,振荡,直至不再有二氧化碳气体产生,然后将混合液转移至分液漏斗中,分去水层,将有机层依次用5mL饱和食盐水和5mL饱和氯化钙溶液洗涤后,转移至锥形瓶中,加入少量无水
向馏出液中缓慢加入5mL饱和碳酸钠溶液,振荡,直至不再有二氧化碳气体产生,然后将混合液转移至分液漏斗中,分去水层,将有机层依次用5mL饱和食盐水和5mL饱和氯化钙溶液洗涤后,转移至锥形瓶中,加入少量无水![]() 固体,静置片刻,过滤除去
固体,静置片刻,过滤除去![]() 固体,然后将有机层进行蒸馏纯化,收集
固体,然后将有机层进行蒸馏纯化,收集![]() 时的馏分,得到
时的馏分,得到![]() 乙酸乙酯。
乙酸乙酯。
请回答下列问题:
(1)实验原理:乙酸与乙醇在催化剂存在的条件下加热可以发生酯化反应生成乙酸乙酯,请用氧同位素示踪法写出CH3CO18OH与CH3CH2OH发生酯化反应的化学方程式。______________。
(2)仪器a的名称为______________,仪器b的规格为_______![]() 填字母
填字母![]() 。
。
A.25 mL B.50mL C.250 mL D.500mL ![]()
(3)步骤![]() 中,将馏出液经饱和碳酸钠溶液处理后的混合液置于分液漏斗中,振荡后静置,水层在________
中,将馏出液经饱和碳酸钠溶液处理后的混合液置于分液漏斗中,振荡后静置,水层在________![]() 填“上层”或“下层”
填“上层”或“下层”![]() 。
。
(4)在步骤![]() 中,加入少量无水硫酸镁固体的作用是__________________________。
中,加入少量无水硫酸镁固体的作用是__________________________。
(5)酯层厚度的标定:加热回流一段时间后再蒸出产物,为了更好地测定有机层厚度,可预先向饱和碳酸钠溶液中加入1滴_________试液,现象是 ___________________。
(6)该实验中乙酸乙酯的产率为_______ (计算结果精确到![]() )。
)。