题目内容
【题目】常温下,向100mL 溶有0.1molCl2的氯水中滴加0.2mol/L 的NaOH 溶液,得到溶液pH 随所加NaOH溶液体积的变化图像如下。下列说法正确的是
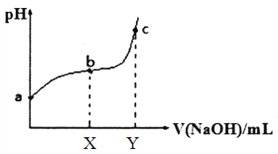
A. a 点有c(H+)=c(ClO-)+c(Cl-)
B. 若x=100,b 点对应溶液中:c(OH-)>c(H+),可用pH 试纸测定其pH
C. 若y=200,c 点对应溶液中:c(OH-)-c(H+)=2c(Cl-)+c(HClO)
D. b~c 段,随NaOH溶液的滴入,![]() 逐渐增大
逐渐增大
【答案】C
【解析】A. a点有电荷守恒:c(H+)=c(ClO-)+c(Cl-)+c(OH-),故A错误;B. 若x=100,Cl2恰好与NaOH溶液生成NaCl、NaClO,NaClO水解生成次氯酸,次氯酸具有漂白性,不能用pH试纸测pH,应选pH计,故B错误;C. 若y=200,c点对应溶液中存在0.1molNaCl、0.1molNaClO、0.2molNaOH,根据电荷守恒得:c(H+)+c(Na+)=c(Cl)+c(ClO)+c(OH)①,氯元素守恒得:c(Cl)=c(ClO)+c(HClO)②,2c(Cl)+2c(ClO)+2c(HClO)=c(Na+)③,由①+③+②得:c(OH)=2c(Cl)+c(HClO)+c(H+),故C正确;D.bc段,Cl2恰好与NaOH溶液生成NaCl、NaClO,随NaOH溶液的滴入,NaOH抑制NaClO水ClO+H2OHClO+OH,c(HClO)减小,c(ClO)增大,所以c(HClO)/c(ClO)减小,故D错误;故选C.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目