��Ŀ����
����Ŀ��ú̿��������Ϊ��ɫ��������������������ʹ�õ���Ҫ��Դ֮һ��Ϊ�����ú�������ʣ������к�������ŷţ����Dz�ȡ�˸�ʽ�����ķ�����
��1��ú��������Һ���������ú�������ʡ�ú��������������Ҫ������___________��ú��Һ�������ַ�Ϊֱ��Һ���ͼ����������ú����������ǿ�ȵõ���¯����ú���ͼ���̿�Ȳ�Ʒ�ļ�����Ϊ___________��
��2��ú��ȼ��ǰ����ȼ�չ����о��ɲ�ȡ��ʩ�����к�������ŷţ�
����ȼ��ǰ�����Բ���������������ԭ�����£�
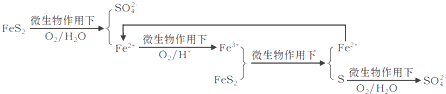
����������Fe2+������Ϊ________________��д��Fe2+![]() Fe3+�����ӷ���ʽ________________��
Fe3+�����ӷ���ʽ________________��
��ú��ȼ��ʱ��������������������________ȼ�ռ������ڰ�ú������������¯ȼ���ң�ʹú����������������г�ֻ�ϡ�ȼ�գ��������ã��������������Ҫ��ѧ�ɷ�Ϊ_______���ѧʽ����
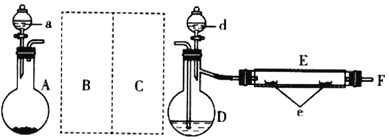
��ú��ȼ�պ��������������ó�����������������������ʪ���������������н�����ͨ��_________�豸����ʯ��ˮ��ϴ��
���𰸡�CO��H2 ú�ĸ��� �м��� �������á��ӿ�SԪ�ص����� 4Fe2++O2+4H+=4Fe3++2H2O ������ CaO������CaCO3�� ������
��������
��1��ú��������ú��ˮ�����ڸ��������·�Ӧ����CO�������Ĺ��̣�����Ҫ����ΪCO��H2����ú����������ǿ��ʹú�ֽ�õ���¯����ú���ͼ���̿�Ȳ�Ʒ�IJ�����ú�ĸ���
��2���ٸ���������������ԭ����֪��Fe2+�ȱ�����ΪFe3+����Fe3+�ֱ���ԭΪFe2+����Fe2+�ȱ����ĺ������ɣ����ڷ�Ӧ����������Fe2+����ԭ��������������ΪFe3+�����������������±���ԭΪH2O���ݴ�д�����ӷ���ʽ��4Fe2++O2+4H+=4Fe3++2H2O���ʴ�Ϊ���м����������ã��ӿ�SԪ�ص�������4Fe2++O2+4H+=4Fe3++2H2O������úȼ�յ�ͬʱ���е���������Ϊ����������ȼ�ռ���������SO2������������ʿ��ԼӼ���������CaO������CaCO3�����������գ�������������װ��Ϊ��������

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
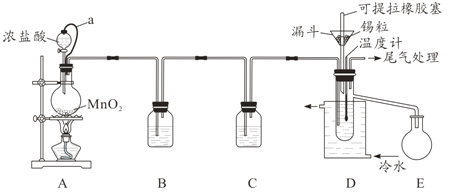
Сѧ��10����Ӧ����ϵ�д�����Ŀ����ˮ���Ȼ���(SnCl4)�������л��ϳɵ��Ȼ�������ʵ���ҿ��������������Ʊ���ˮ���Ȼ�����ʵ��װ��ͼ��ͼ��
�������Ͽ�֪��
��Sn(s)+2Cl2(g)=SnCl4(l) ��H=-511kJ/mol
��SnCl4�ӷ���������ˮ�⡣
��������ʵ������������£�
���� | Sn | SnCl4 | CuCl2 |
�۵�/�� | 232 | -33 | 620 |
�е�/�� | 2260 | 114 | 993 |
�ܶ�/g��cm-3 | 7.310 | 2.226 | 3.386 |
�ش��������⣺
(1)a�ܵ�������__________��
(2)A�з�Ӧ�����ӷ���ʽ��__________��
(3)D����ȴˮ��������________________��
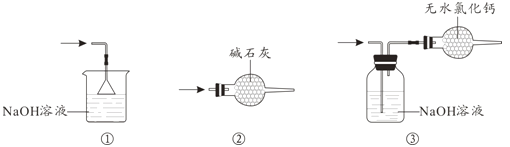
(4)β������ʱ����ѡ�õ�װ����__________(�����)��
(5)�����к�ͭ������D�в���CuCl2������Ӱ��E�в�Ʒ�Ĵ��ȣ�ԭ����________��
(6)�Ƶõ�SnCl4��Ʒ�г�����SnCl2���������·����ⶨ��Ʒ���ȣ���ȷ����7.60g��Ʒ����ƿ�У��ټӹ�����FeCl3��Һ��������Ӧ��SnCl2+2FeCl3=SnCl4+2FeCl2������0.1000mol/LK2Cr2O7����Һ�ζ����ɵ�Fe2+����ʱ��ԭ����ΪCr3+�����ı���Һ20.00mL����SnCl4��Ʒ�Ĵ���Ϊ__________��
����Ŀ���ҹ����Ϻ�����������еĿ�ȼ���Բɳɹ������־���ҹ���Ϊȫ���һ��ʵ�����ں����ȼ���Կ����л�������ȶ������Ĺ��ҡ���ȼ����Ҫ�ɷ��Ǽ��飬��������ȼ�Ϻ�����ԭ�ϡ����������������Ƚ������ⷽ���������������������������������̡���������Ҫ��Ӧ���£�
��ѧ����ʽ | �ʱ���H/��kJ��mol-1�� | ���Ea/��kJ��mol-1�� | |
�������� | CH4��g����2O2��g�� | -802.6 | 125.6 |
CH4��g����O2��g�� | -322.0 | 172.5 | |
�������� | ��CH4��g����H2O��g�� | ��206.2 | 240.1 |
��CH4��g����2H2O��g�� | ��165 | 243.9 |
����˵������ȷ����
A.CO��g����H2O��g��![]() CO2��g����H2��g�� ��H����41.2kJ��mol-1
CO2��g����H2��g�� ��H����41.2kJ��mol-1
B.��Ӧ���淴Ӧ���Ea��78.9kJ��mol-1
C.��ʼ�Σ��������������ʴ��ڼ�����������������
D.������������������ͻ���ŵ�������ѭ������
����Ŀ�����³�ѹ�£�����֧��ͬ���Թ��У��ֱ�װ������ʵ�����ϵ��������塣����������������£�
�Թܱ�� | 1 | 2 | 3 | 4 |
���������� | Cl2��SO2 | NO2��O2 | NO��O2 | NH3��N2 |
����֧�Թ�Ѹ��ͬʱ������ˮ���У���Һ���ȶ���ˮ�������߶��ɴ�С��ȷ���ǣ� ��
A.1��2��3��4B.3��1��4��2
C.4��2��3��1D.1��3��2��4