题目内容
向容积为2L的密闭容器中充入2mol X气体和1mol Y气体,在一定条件下发生如下反应:2X(g)+Y(g)?3R(g),该反应经2s后达到平衡,测得R气体的浓度为0.6mol/L.下列说法中错误的是( )
分析:A、R的浓度变化为0.6mol/L,根据v=
计算v(R),根据速率之比等于化学计量数之比计算v(X);
B、依据反应前后气体体积不变,加入R气体平衡体系总压增大,平衡不动分析;
C、其他条件不变,加压缩小容器体积时,反应前后气体体积不变,所以平衡不移动,气体质量不变,物质的量不变,体积减小气体密度增大,平均相对分子质量不变;
D、x、y化学计量数之比为2:1,参加反应的x、y的物质的量之比为2:1,x、y的起始物质的量之比为2:1,平衡时物质A与B的转化率相等.
| △C |
| △t |
B、依据反应前后气体体积不变,加入R气体平衡体系总压增大,平衡不动分析;
C、其他条件不变,加压缩小容器体积时,反应前后气体体积不变,所以平衡不移动,气体质量不变,物质的量不变,体积减小气体密度增大,平均相对分子质量不变;
D、x、y化学计量数之比为2:1,参加反应的x、y的物质的量之比为2:1,x、y的起始物质的量之比为2:1,平衡时物质A与B的转化率相等.
解答:解:2X(g)+Y(g)?3R(g),反应是气体体积不变的反应;
A、R的浓度变化为0.6mol/L,根据v=
计算v(R)=
=0.3mol/L?s,根据速率之比等于化学计量数之比计算v(X)=
×v(R)=
×0.3mol/L?s=0.2mol/L?s,故A正确;
B、依据反应前后气体体积不变,加入R气体平衡体系总压增大,达到新的平衡后平衡不动,R的体积分数不变,故B正确;
C、其他条件不变,加压缩小容器体积时,反应前后气体体积不变,所以平衡不移动,气体质量不变,物质的量不变,体积减小气体密度增大,平均相对分子质量不变,故C错误;
D、x、y化学计量数之比为2:1,参加反应的x、y的物质的量之比为2:1,x、y的起始物质的量之比为2:1,平衡时物质A与B的转化率相等,故D正确;
故选C.
A、R的浓度变化为0.6mol/L,根据v=
| △C |
| △t |
| 0.6mol/L |
| 2s |
| 2 |
| 3 |
| 2 |
| 3 |
B、依据反应前后气体体积不变,加入R气体平衡体系总压增大,达到新的平衡后平衡不动,R的体积分数不变,故B正确;
C、其他条件不变,加压缩小容器体积时,反应前后气体体积不变,所以平衡不移动,气体质量不变,物质的量不变,体积减小气体密度增大,平均相对分子质量不变,故C错误;
D、x、y化学计量数之比为2:1,参加反应的x、y的物质的量之比为2:1,x、y的起始物质的量之比为2:1,平衡时物质A与B的转化率相等,故D正确;
故选C.
点评:本题考查了化学平衡、化学反应速率影响因素分析判断,化学反应速率的计算应用和反应物转化率的比较,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
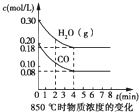 某研究小组利用反应CO(g)+H2O(g)?CO2(g)+2H2(g)△H=-41.2kJ/mol,制备CO2与H2的混合气体,并进一步研究CO2与H2以不同的体积之比混合时在合适条件下的反应情况.请回答下列问题:
某研究小组利用反应CO(g)+H2O(g)?CO2(g)+2H2(g)△H=-41.2kJ/mol,制备CO2与H2的混合气体,并进一步研究CO2与H2以不同的体积之比混合时在合适条件下的反应情况.请回答下列问题: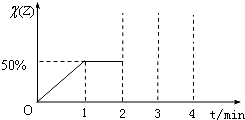

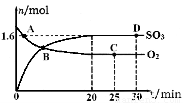
 2SO3(g) ∆H=-akJ/mol(a>0),经2min达到平衡状态,反应放热0.25akJ。下列判断正确的是
2SO3(g) ∆H=-akJ/mol(a>0),经2min达到平衡状态,反应放热0.25akJ。下列判断正确的是