题目内容
【题目】(1)现有以下物质①熔融状态的NaCl ②NH3·H2O ③Na2O固体 ④铜 ⑤BaSO4固体 ⑥酒精 ⑦液态HCl ⑧KNO3溶液,其中属于电解质的是:___________;该状态下能导电的是_____________;属于非电解质的是_________________。(请用序号作答)
(2)以下A~D四个涉及H2O2的反应,请填空:
A. Na2O2+ 2HCl=H2O2+2NaCl B. Ag2O+H2O2=2Ag+O2↑+H2O
C. 2H2O2=2H2O+O2↑ D. □H2O2+□KMnO4+□H2SO4→□MnSO4+□K2SO4+□H2O+□O2↑
①配平D方程式,系数填在方框内____;该反应的还原剂是_________________;
②H2O2既体现氧化性,又体现还原性的反应是________,H2O2既不作氧化剂又不作还原剂的反应是__________。(请用代号作答)
③请用双线桥法表示B反应中电子转移的方向和数目:___________。
【答案】 ①②③⑤⑦ ①④⑧ ⑥ 2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O H2O2 C A 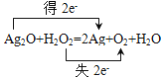
【解析】(1)水溶液中或熔化状态下能导电的化合物为电解质,则以上几种物质中,只有①②③⑤⑦为电解质,存在自由移动的离子或电子的物质能导电,则以上几种物质中只有①④⑧能导电,水溶液中和熔化状态下都不能导电的化合物为非电解质,则以上几种物质中,属于非电解质的有⑥,故答案为:①②③⑤⑦;①④⑧;⑥;
(2)①KMnO4中Mn的化合价为+7价,反应后变成了MnSO4,化合价变成+2,Mn元素化合价降低被还原,化合价降低了5价;H2O2中氧元素化合价为-1价,反应后变成了0价的O,化合价升高了1价,1分子双氧水反应,至少化合价升高2价,化合价变化的最小公倍数为10,所以KMnO4的计量数为2,双氧水的计量数为5,然后利用观察法配平其它物质,配平后的方程式为2KMnO4+5H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O,反应中双氧水中的O被氧化,双氧水为还原剂,故答案为:2KMnO4+5H2O2+3H2SO4= K2SO4+2MnSO4+5O2↑+ 8H2O;H2O2;
②A.Na2O2+2HCl=H2O2+2NaCl,是一个非氧化还原反应,双氧水既不是氧化剂,也不是还原剂;B.Ag2O+H2O2=2Ag+O2+H2O,Ag2O被还原成单质银,H2O2仅表现为还原性,其中氧元素转化为O2;C.2H2O2=2H2O+O2↑,过氧化氢的分解反应,是一个自身氧化还原反应,H2O2既表现了氧化性,又表现了还原性;D.H2O2+KMnO4+H2SO4→ MnSO4+K2SO4+H2O+O2↑,双氧水在反应中O元素的化合价由-1变成0,化合价升高被氧化,双氧水仅做还原剂;所以H2O2既体现氧化性,又体现还原性的反应是C;H2O2既不做氧化剂又不做还原剂的反应是A,故答案为:C;A;
③Ag2O+H2O2=2Ag+O2+H2O,Ag2O被还原成单质银,得2e-;H2O2仅表现为还原性,其中氧元素转化为O2;失2e-,反应中电子转移的方向和数目用双线桥法表示为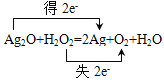 ,故答案为:
,故答案为: 。
。

 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案