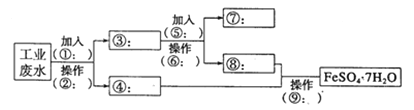
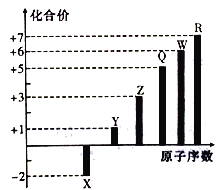
��Ŀ����
����Ŀ����ͼ���߿��е�װ��(�Լ�������)����������Ũ������ľ̿���ڼ��������·�Ӧ����������������������˵����ȷ����
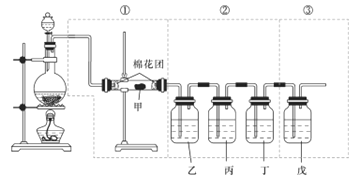
A. ���ʼ�������ˮ����ͭ����ɫ�轺����ˮ�Ȼ��Ƶ�����
B. ���з�����Ӧ�����ӷ���ʽ������SO2+2OH-=SO32-+H2O
C. �Һ���������Һ����������β������װ���е��Լ�
D. �����װ�õ�����˳���Ϊ�٢ۢڣ���ֻ�ܼ�������ֲ���
���𰸡�C
��������̼��Ũ���ᷴӦ�ķ���ʽΪ��C+2H2SO4��Ũ��![]() 2SO2��+CO2��+2H2O��SO2��ʹƷ����Һ��ɫ��SO2Ҳ��ʹ���Ը��������Һ��ɫ��ͨ�����Ը��������Һ��ȥSO2��CO2����ʹƷ����Һ��ɫ��CO2Ҳ�������Ը��������Һ��ɫ����ˮ����ͭ��ˮ������������������̼����ʹ����ʯ��ˮ����ǣ���A��װ�â��Ǽ������������Ƿ���ˮ������Ӧ������ˮ����ͭ����ɫ�轺����������ˮ�Ȼ��ƣ�A����B��������̼Ҳ�ܱ�����������Һ���գ������Լ�Ӧ�������Ը��������Һ��B����C��Ʒ����Һ���Լ����������һ�㲻��������ȥ����������ʯ��ˮŨ��̫С�������������ն�������C��ȷ��D�����������������˳���Ϊ�١��ۡ��ڣ�ͨ������װ����ˮ����ͭ����ˮ����ͭ��ˮ�ɰ�ɫ�����ɫ����˵����ˮ���ɣ�ͨ���۳���ʯ��ˮ��ʯ��ˮ����ǣ�������������̼����ʹ����ʯ��ˮ����ǣ������Լ��������������̼��D����ѡC��
2SO2��+CO2��+2H2O��SO2��ʹƷ����Һ��ɫ��SO2Ҳ��ʹ���Ը��������Һ��ɫ��ͨ�����Ը��������Һ��ȥSO2��CO2����ʹƷ����Һ��ɫ��CO2Ҳ�������Ը��������Һ��ɫ����ˮ����ͭ��ˮ������������������̼����ʹ����ʯ��ˮ����ǣ���A��װ�â��Ǽ������������Ƿ���ˮ������Ӧ������ˮ����ͭ����ɫ�轺����������ˮ�Ȼ��ƣ�A����B��������̼Ҳ�ܱ�����������Һ���գ������Լ�Ӧ�������Ը��������Һ��B����C��Ʒ����Һ���Լ����������һ�㲻��������ȥ����������ʯ��ˮŨ��̫С�������������ն�������C��ȷ��D�����������������˳���Ϊ�١��ۡ��ڣ�ͨ������װ����ˮ����ͭ����ˮ����ͭ��ˮ�ɰ�ɫ�����ɫ����˵����ˮ���ɣ�ͨ���۳���ʯ��ˮ��ʯ��ˮ����ǣ�������������̼����ʹ����ʯ��ˮ����ǣ������Լ��������������̼��D����ѡC��

 �����ߴ���ϵ�д�
�����ߴ���ϵ�д�����Ŀ����ˮ���Ȼ���(SnCl4) ʵ���ҿ������ڵ���(�۵�Ϊ23.9��)��Cl2��Ӧ�Ʊ�SnCl4��װ������ͼ��ʾ�ش�����������

��֪SnCl4��ʪ�����м���ˮ������SnO2��xH2O��
���� | ��ɫ��״̬ | �۵�/�� | �е�/�� |
SnCl2 | ��ɫ���� | 246 | 652 |
SnCl4 | ��ɫҺ�� | -33 | 114 |
��1��a�ܵ�������________��װ��A�з�����Ӧ�Ļ�ѧ����ʽ��______________��
��2��װ��B��C��F��G��ʢ�ŵ�����Լ�����Ϊ____________(����ţ��Լ����ظ�ʹ��)��
�ٱ���Na2CO3��Һ ��NaOH��Һ ��ŨH2SO4 ������NaCl��Һ ��H2O
��3����ȼ�ƾ���ǰ��Ҫ���е�һ��������______________��
��4������ȥװ��C����װ��D�п��ܻᷢ������Ҫ����Ӧ�Ļ�ѧ����ʽΪ___________��
��5���õ��IJ����г�����SnCl2��ijʵ��С���õ��������ζ�������Ʒ��SnCl4�ĺ���(Sn2++I2=Sn4++2I-)��ȷ��ȡmg��Ʒ����ƿ�У�������Ũ�����ܽ⣬�ټ�ˮϡ�ͣ�������Һ��ָʾ������0.1mol/L�����Һ�ζ����յ㣬�ﵽ�ζ��յ�ʱ������Ϊ________�����ĵ����Һ20.00mL�������Ʒ��SnCl4�ĺ���______(�ú�m�Ĵ���ʽ��ʾ)��