题目内容
常温下,pH都等于9的NaOH溶液和CH3COONa两种溶液中,若由水电离产生OH- 浓度分别为a mol/L和b mol/L,则a和b的关系是
| A.a>b | B.a=10-4b | C.b=10-4a | D.a=b |
B
解析试题分析:根据H2O H++OH-,从影响水的电离平衡移动的角度分析,NaOH抑制水的电离,CH3COONa促进水的电离,据此可以解答。pH=9的NaOH溶液,由NaOH电离产生的c(OH-)=10-5mol/L,则由水电离产生的c(OH-)=c(H+)=
H++OH-,从影响水的电离平衡移动的角度分析,NaOH抑制水的电离,CH3COONa促进水的电离,据此可以解答。pH=9的NaOH溶液,由NaOH电离产生的c(OH-)=10-5mol/L,则由水电离产生的c(OH-)=c(H+)= mol/L=10-9mol/L,即a=10-9mol/L;pH=9的CH3COONa溶液促进水的电离,OH-全部由水电离产生,c(OH-)=10-5mol/L,即b=c(OH-)=10-5mol/L,所以a:b=10-9mol/L:10-5mol/L=10-4,即a=10-4b,答案选B。
mol/L=10-9mol/L,即a=10-9mol/L;pH=9的CH3COONa溶液促进水的电离,OH-全部由水电离产生,c(OH-)=10-5mol/L,即b=c(OH-)=10-5mol/L,所以a:b=10-9mol/L:10-5mol/L=10-4,即a=10-4b,答案选B。
考点:考查水的电离、离子积常数和pH的计算

 金状元绩优好卷系列答案
金状元绩优好卷系列答案在25 ℃时,用蒸馏水稀释1 mol·L-1氨水至0.01 mol·L-1,随溶液的稀释,下列各项中始终保持增大趋势的是( )
| A.c(NH4+)/c(OH-) | B.c(OH-)/c(NH3·H2O) |
| C.c(NH3·H2O)/c(NH4+) | D.OH-物质的量 |
在足量锌与等物质的量浓度、等体积的盐酸和醋酸反应时,下列叙述正确的是
| A.开始反应时,二者的速率相等 | B.盐酸放出的H2多 |
| C.二者放出的H2一样多 | D.醋酸消耗的Zn的质量多 |
25℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH 的关系如图所示。下列有关溶液中离子浓度关系叙述正确的是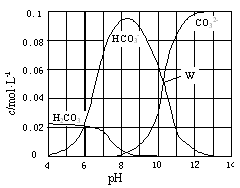
| A.W点所示的溶液中:c(Na+)+ c(H+)=2c(CO32-)+ c(OH-)+ c(Cl-) |
| B.pH=4的溶液中:c(H2CO3)+ c(HCO3-)+ c(CO32-)<0.1 mol·L-1 |
| C.pH=8的溶液中:c(H+)+ c(H2CO3)+ c(HCO3-) = c(OH-)+c(Cl-) |
| D.pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)>c(H2CO3) |
下列离子方程式中,属于水解反应的是
A.HCOOH+H2O HCOO-+H3O+ HCOO-+H3O+ | B.CO2+H2O HCO-3+H+ HCO-3+H+ |
C.CO32-+ H2O HCO-3+OH- HCO-3+OH- | D.HS- S2-+H+ S2-+H+ |
下列实验,不能说明乙酸是弱电解质的是
| A.常温时,测得乙酸钠溶液的pH>7 |
| B.常温时,测得0.1 mol·L-1乙酸溶液的pH约为3 |
| C.乙酸溶液与大理石反应产生气泡 |
| D.相同温度下,测得同物质的量浓度的乙酸溶液的导电性比盐酸溶液弱 |
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是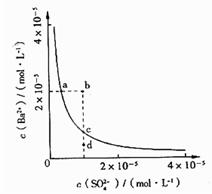
提示:BaSO4(s) Ba2+(aq)+SO42-(aq)的平衡常数 Ksp=c(Ba2+)·c(SO42-),称为溶度积常数。
Ba2+(aq)+SO42-(aq)的平衡常数 Ksp=c(Ba2+)·c(SO42-),称为溶度积常数。
| A.加入Na2SO4可以使溶液由a点变到b点 |
| B.通过蒸发可以使溶液由d点变到c点 |
| C.d点无BaSO4沉淀生成 |
| D.a点对应的Ksp大于c点对应的Ksp |
氢氟酸为弱酸。250C时将0.1mol·L-1的HF加水不断稀释,下列表示的量保持不变的是
①n(H+);②c(H+)·c(OH—);③c(OH—)+ c(F—);④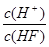 ;⑤
;⑤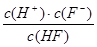 ;
;
| A.①③④ | B.②③④ | C.③④⑤ | D.②⑤ |
已知常温时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=12.0,则下列说法不正确的是 ( )
| A.所得溶液中的c(H+)=1.0×10-12 mol·L-1 |
| B.所加的烧碱溶液pH=12.0 |
| C.所得溶液中由水电离产生的c(OH-)=1.0×10-12 mol·L-1 |
| D.所得溶液中的c(Mg2+)=5.6×10-8 mol·L-1 |