题目内容
用质量分数为98%、密度为1.84g·cm-3的浓硫酸配制100mL1.84mol·L-1的稀硫酸,若实验仪器有:A.100mL量筒;B.托盘天平;C.玻璃棒;D.50mL容量瓶;E.10mL量筒,F.胶头滴管;G.50mL烧杯;H.100mL容量瓶,
a.实验时应选用仪器的先后顺序是(填入编号): 。
b.在容量瓶的使用方法中,下列操作不正确的是(填编号)________。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线2~3cm处,用滴管加蒸馏水到标线
D.配制溶液时,如果试样是液体,用量筒量取试样后,直接倒入容量瓶中,缓慢加入蒸馏水到标线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
F.往容量瓶中转移溶液时应用玻璃棒引流
c.在配制溶液时,下列操作出现的后果是(填:“偏低”、“偏高”、“无影响”):
(1)配制硫酸溶液时,容量瓶中有少量水。 ______________。
(2)未洗涤烧杯和玻璃棒。__________。
(3)配制好溶液、摇匀后,容量瓶未塞好,洒出一些溶液。_____________。
(4)定容时,俯视读数。________________。
(5)定容时,液面上方与刻度相齐时,停止加水。________________。
(6)定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。____________。
(a)EFGCHF (3分) (b)BCD (3分)(c)(每空2分)
(1)无影响 (2) 偏低 (3)无影响 (4) 偏高 (5)偏高(6)偏低
【解析】(a)浓硫酸配制稀硫酸,则需要量筒和胶头滴管量取溶液的体积;稀释需要烧杯和玻璃棒,转移需要玻璃棒和容量瓶;定容需要胶头滴管。经计算需要浓硫酸的体积是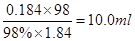 ,所以选择10ml量筒,因此正确的答案选EFGCHF。
,所以选择10ml量筒,因此正确的答案选EFGCHF。
(b)容量瓶不能用待配的溶液洗涤,B不正确;容量瓶也不能用来稀释,C不正确;液体也需要稀释后在转移至容量瓶中,D不正确,所以正确的答案选BCD。
(c)根据c=n/V可知;(1)容量瓶中有少量水,不影响浓度大小。
(2)未洗涤烧杯和玻璃棒,则溶质减少,浓度降低。
(3)容量瓶未塞好,洒出一些溶液,但由于已经配制完毕,所以没有影响。
(4)定容时,俯视读数,则容量瓶中溶液体积减少,浓度偏高。
(5)定容时,液面上方与刻度相齐时,停止加水,则容量瓶中溶液体积偏少,浓度偏高。
(6)定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度,则容量瓶中溶液体积偏大,所以浓度偏低。

 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案 欲用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制0.2mol/L的硫酸溶液480mL.试回答下列问题:
欲用质量分数为98%、密度为1.84g/cm3的浓硫酸,配制0.2mol/L的硫酸溶液480mL.试回答下列问题: