题目内容
15.下列说法不正确的是( )| A. | 检验Cl-的试剂是硝酸银和硝酸 | |
| B. | 检验SO42-的试剂是氯化钡和盐酸 | |
| C. | 向某溶液中滴加盐酸,生成使澄清石灰水变浑浊的无色无味的气体,则该溶液中含有CO32-或HCO32- | |
| D. | 向溶液中加入氯化钡溶液后生成白色沉淀,即可证明有SO42- |
分析 A.检验Cl-的试剂是硝酸银和稀硝酸;
B.检验SO42-,先加入稀盐酸,无明显现象,再加入氯化钡溶液;
C.使澄清石灰水变浑浊的无色无味的气体为二氧化碳,原溶液中可能还有碳酸根离子或碳酸氢根离子;
D.向溶液中加入BaCl2溶液后生成白色沉淀,可能是CO32-.
解答 解:A.检验Cl-,加入硝酸银和稀硝酸,若有白色沉淀生成,证明含有Cl-,故A正确;
B.检验SO42-的方法为:先加入稀盐酸,无明显现象,再加入氯化钡溶液,若有白色沉淀生成,证明含有SO42-,故B正确;
C.某溶液中滴加盐酸,生成使澄清石灰水变浑浊的无色无味的气体,该气体为二氧化碳,则该溶液中含有CO32-或HCO32-,故C正确;
D.向溶液中加入BaCl2溶液后生成白色沉淀,可能是CO32-,不一定是SO42-,故D错误;
故选D.
点评 本题考查了常见离子的检验方法,题目难度中等,明确常见离子的性质及检验方法为解答关键,注意熟练掌握常见离子,如氯离子、硫酸根等离子的检验方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.在体积不变的密闭容器中充入1mol NH3,发生反应2NH3?3H2+N2,并达到平衡状态,测得NH3的转化率为x%.若在其他条件不变时,再充入1mol NH3,待建立新的平衡后,测得NH3的转化率为y%,则x和y的正确关系为( )
| A. | x>y | B. | x<y | C. | x=y | D. | x≥y |
3.根据电离平衡原理,设计实验证明NH3•H2O是弱碱.
可选用的试剂:酚酞、石蕊、稀氨水、醋酸铵晶体和蒸馏水.
可选用的试剂:酚酞、石蕊、稀氨水、醋酸铵晶体和蒸馏水.
| 实验操作 | 实验现象 |
| ①取少量氨水于试管中,滴加酚酞试液 ②向试管中加入少量醋酸铵晶体,振荡 | 溶液呈红色 红色变浅 |
| 结论:氨水中存在电离平衡,证明氨水是弱碱 | |
10.常温下,下列溶液中氢离子浓度最小的是( )
| A. | pH=0的NaHSO4溶液 | B. | 0.04 mol•L-1 硫酸 | ||
| C. | 0.5 mol•L-1 盐酸 | D. | 0.05 mol•L-1硝酸 |
4.对于X+Y(s)?Z的平衡,若增大压强,Y的转化率增大,则X和Y的状态是( )
| A. | X为气态,Z为固态 | B. | X为固态,Z为气态 | C. | X为气态,Z为气态 | D. | X为固态,Z为固态 |
5.当光速通过下列分散系:①豆浆 ②混有尘埃的空气 ③稀盐酸 ④蒸馏水 能观察到有丁达尔效应的是( )
| A. | ①③ | B. | ②④ | C. | ①② | D. | ①④ |
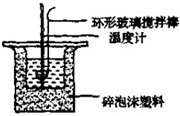 实验室利用右图装置进行中和热的测定,请回答下列问题:
实验室利用右图装置进行中和热的测定,请回答下列问题: