题目内容
【题目】为探究某矿石(仅含两种元素)的组成和性质,设计并完成如下实验:
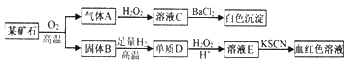
请回答:(1)某矿石的组成元素为__________(用元素符号表示)。
(2)气体A与H2O2溶液反应的化学方程式是________________。
(3)写出D→E的离子方程式____________________。
【答案】 Fe、S SO2+H2O2=H2SO4 2Fe+3H2O2+6H+=2Fe3++6H2O
【解析】溶液E与KSCN溶液作用溶液显血红色,说明E中含有铁离子,E由单质在酸性条件下与双氧水发生氧化还原反应而得到,故D为铁;固体B应该为铁的氧化物,与足量氢气在高温条件下被还原生成铁;气体A应该是二氧化硫,在双氧水作用下生成C为硫酸,硫酸与氯化钡反应生成白色沉淀硫酸钡。故某矿石应该含有铁、硫两种元素。(1)某矿石的组成元素为Fe、S;(2)气体A与H2O2溶液反应的化学方程式是SO2+H2O2=H2SO4;(3) D→E为铁在酸性条件下被双氧水氧化生成铁盐和水,其离子方程式为:2Fe+3H2O2+6H+=2Fe3++6H2O。

【题目】一定温度下,在2.5L的恒容密闭容器中发生如下反应:CO2(g)+H2S(g)![]() COS(g)+H2O(g)
COS(g)+H2O(g)
实验 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 | |
CO2 | H2S | H2O | |||
I | 607 | 0.11 | 0.41 | 0.01 | |
II | 607 | 0.22 | 0.82 | ||
III | 620 | 0.1 | 0.4 | 6.74×10-3 | |
下列说法不正确的是( )
A. 该反应正反应为吸热反应
B. 607K时,把物质的量均为0.1mol四种反应物加入该反应器中,反应将向正反应方向进行
C. 实验Ⅱ达到平衡时容器中COS的物质的量为0.02mol
D. 实验Ⅲ中,无论是开始还是至化学平衡状态,混合气体的密度始终不变