题目内容
【题目】.实验室要配制240mL 0.2mol·L-1的Na2CO3溶液,试回答下列各题:
(1)若用Na2CO3固体配制溶液,下列仪器中,不需要用到的是______________。
A.锥形瓶 B.200mL容量瓶 C.烧杯 D.胶头滴管
E.药匙 F.托盘天平 G.洗瓶 H.试剂瓶
(2)若要实施配制,除上述仪器外,尚缺的必须的仪器是________________________。
(3)需要称量Na2CO3固体的质量是____________________________ 。
(4)下列四项操作会导致所得溶液浓度偏高的是__________。
a.容量瓶不干燥
b.定容时俯视容量瓶刻度线
c.称量Na2CO3固体时物体和砝码放反了(1克以下用游码)
d.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
【答案】AB 250mL容量瓶、玻璃棒 5.3g b
【解析】
根据配制溶液的步骤分析需要的仪器;配制240mL 0.2mol·L-1的Na2CO3溶液,应选择250mL容量瓶,配制250mL溶液;根据![]() 分析实验误差。
分析实验误差。
(1)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶保存,用到的仪器:托盘天平、药匙、烧杯、玻璃棒、容量瓶、胶头滴管、试剂瓶,配制240mL 0.2mol·L-1的Na2CO3溶液,应选择250mL容量瓶,用不到的仪器是锥形瓶和200mL容量瓶,故选AB;
(2)根据(1)的分析,若要实施配制,除上述仪器外,尚缺的必须的仪器是250mL容量瓶、玻璃棒;
(3)应选择250mL容量瓶,配制250mL溶液,需要称量Na2CO3固体的质量是0.2mol·L-1×0.25L×106g/mol=5.3g;
(4)a.需要加水定容,所以容量瓶不干燥,对实验无影响,故不选a;
b.定容时俯视容量瓶刻度线,所配溶液体积偏小,所得溶液浓度偏高,故选b;
c.称量Na2CO3固体时物体和砝码放反了(1克以下用游码),称取碳酸钠质量偏小,所得溶液浓度偏低,故不选c;
d.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处,所配溶液体积偏大,所得溶液浓度偏低,故不选d;
答案为b。

【题目】盐酸与碳酸钙反应生成CO2,运用下图,可测定该反应的速率.请根据要求填空:
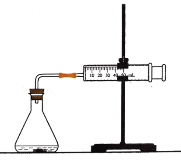
(1)连接好仪器后,需要检查_____________________,再加入药品进行实验.
(2)在锥形瓶中加入5g大理石,加入20mL 1mol·L1盐酸.每隔10s观测玻璃注射器中气体的体积,并以mL·s1为反应速率的单位,计算每10s时间间隔内的反应速率。数据处理的结果见下面的表格:
时间/s | 10 | 20 | 30 | 40 | 50 | 60 |
气体体积/mL | 4 | 14 | 25 | 38 | 47 | 55 |
反应速率/mL·s1 | 0.4 | 1.0 | 1.1 | ? | 0.9 | 0.8 |
表格中的“?”处应填的数据是_________________.
(3)从反应速率随时间变化的数据可知,本实验中反应速率与___________和__________有关