题目内容
【题目】如下图所示(B中冷却装置未画出),将氯气和空气(不参与反应)以体积比约1:3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O制备次氯酸溶液。
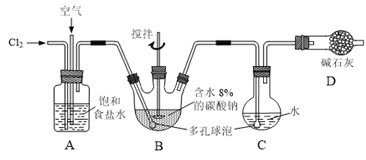
已知:Cl2O极易溶于水并与水反应生成HClO;Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2。
(1)①实验中控制氯气与空气体积比的方法是______。
②为使反应充分进行,实验中采取的措施有______。
(2)①写出装置B中产生Cl2O的化学方程式并用单线桥法标出电子转移的方向和数目:______。
②若B无冷却装置,则进入C中的Cl2O会大量减少。其原因是______。
(3)装置C中采用棕色圆底烧瓶是因为______。
(4)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定C中次氯酸溶液的物质的量浓度的实验方案为:用酸式滴定管准确量取20.00 mL次氯酸溶液,______。(可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液。除常用仪器外须使用的仪器有:电子天平,真空干燥箱)
【答案】 通过观察A中产生气泡的速率调节流速 搅拌、使用多孔球泡 ![]() 该反应放热,温度升高Cl2O会分解 HClO见光易分解 加入足量的H2O2溶液,再加入足量的硝酸银溶液,过滤,洗涤,在真空干燥箱中干燥,用电子天平称量沉淀质量
该反应放热,温度升高Cl2O会分解 HClO见光易分解 加入足量的H2O2溶液,再加入足量的硝酸银溶液,过滤,洗涤,在真空干燥箱中干燥,用电子天平称量沉淀质量
【解析】(1)①氯气和空气按照体积比约1:3混合通入潮湿碳酸钠中,控制氯气与空气体积比的方法可以通过观察A中产生气泡的比例来调节气体的流速,故答案为:通过观察A中产生气泡的速率调节流速;
②为了氯气和原溶液充分接触完全反应,可以通过增加气体与溶液的接触面积、并用搅拌棒搅拌等方法,故答案为:搅拌、使用多孔球泡;
(2)①装置B中,氯气本身既作为氧化剂又作还原剂,被氧化到+1价的Cl2O,被还原到-1价的氯化钠,故化学方程式为2Cl2+Na2CO3═Cl2O+2NaCl+CO2,用单线桥法标出电子转移的方向和数目表示为:![]() ,故答案为:
,故答案为:![]() ;
;
(4)由于该反应为放热反应,温度升高Cl2O会分解,故进入C中的Cl2O会大量减少,故答案为:该反应放热,温度升高Cl2O会分解;
(3)装置C中使用棕色平底烧瓶,目的是可以避光,防止反应生成的HClO见光分解,故答案为:HClO见光易分解;
(4)选择使用酸式滴定管量取20.00mL的次氯酸溶液,具体实验操作是,向20.00mL的次氯酸溶液里加入足量的H2O2溶液,再加入足量的硝酸银溶液,过滤、洗涤,在真空干燥箱中干燥沉淀,用电子天平称量沉淀的质量,故答案为:加入足量的H2O2溶液,再加入足量的硝酸银溶液,过滤,洗涤,在真空干燥箱中干燥,用电子天平称量沉淀质量。

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案