题目内容
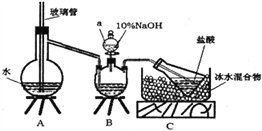
【题目】二氧化氯是一种广谱杀菌消毒剂,有众多的用途,工业上制取二氧化氯的化学方程式如下:2NaClO3+ 2NaCl+2H2SO4![]() 2ClO2↑+Cl2↑+2H2O+2Na2SO4。
2ClO2↑+Cl2↑+2H2O+2Na2SO4。
(1)完成下列计算:0.2 mol NaClO3完全反应,得到气体的体积为__________L(标准状况)。
(2)将27.0 g ClO2溶于水得0.5 L溶液,则ClO2的物质的量浓度为__________mol/L。
(3)为使上述反应产生的Cl2转化为ClO2,将得到的混合气体和NaClO2反应,反应方程式为:2NaClO2 + Cl2![]() 2ClO2+2NaCl。假设NaClO3的转化率为90%,Cl2的转化率为95%,计算由0.2 mol NaClO3最终可制得的ClO2的质量(保留两位小数)_____。
2ClO2+2NaCl。假设NaClO3的转化率为90%,Cl2的转化率为95%,计算由0.2 mol NaClO3最终可制得的ClO2的质量(保留两位小数)_____。
【答案】 6.72 0.8 23.70 g
【解析】
试题(1)从反应分析2摩尔铝酸钠反应生成1摩尔氯气,所以当0.2摩尔铝酸钠反应生成0.1摩尔氯气和0.2摩尔二氧化氯,总共0.3摩尔气体,标况下的体积为0.3×22.4=6.72L。
(2)27.0克二氧化氯的物质的量为27.0/67.5=0.4摩尔,其物质的量浓度为0.4/0.5=0.8mol/L。(3)根据方程式找出关系式为:2NaClO3~~ 2ClO2↑~~~ Cl2↑~2NaClO2~~~~2 ClO2,0.2摩尔铝酸钠反应转化率为90%,生成二氧化氯的物质的量为0.2×90%=0.18摩尔,生成的氯气为0.09摩尔,则氯气再与NaClO2反应生成二氧化氯,转化率为95%,则生成的二氧化氯为0.09×2×95%=0.171摩尔,则二氧化氯的物质的量总共为0.18+0.171=0.351摩尔,其质量为0.351×67.5=23.70克。

【题目】某研究性学习小组同学为了探究“在相同的温度和压强下、相同体积的任何气体都含有相同数目和分子”,他们设计了如下实验装置并记录相关实验数据。实验装置:
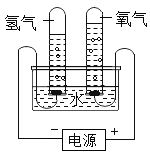
部分实验数据:
温度 | 压强 | 时间 | 水槽中H2O的质量 | H2体积 | O2体积 |
30℃ | 101 kPa | 0 | 300 g | 0 | 0 |
30℃ | 101 kPa | 4分钟 | 298.2 g | 1.243 L |
请回答下列问题:
(1)4分钟时H2、O2物质的量分别是__________mol、___________mol。
(2)该温度下,气体摩尔体积是________________。
(3)假设电解H2O速率相同,2分钟时试管内收集到的H2的体积是___________mL。
(4)根据以上实验得出如下结论,其中不正确的是_________________。
A. 气体摩尔体积与气体的温度相关
B. 在该实验条件下,3 mol O2的气体摩尔体积为74.58 L/mol
C. 同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D. 该实验条件下,O2的密度为1.287 g/L