题目内容
【题目】下列物质中,常用作还原剂的是
A.氯气B.金属钠C.氯化铁D.二氧化硅
【答案】B
【解析】
A. 氯气具有强氧化性,一般用作氧化剂,A不符合题意;
B. 金属钠中Na元素化合价为0价,容易失去电子,表现还原性,作还原剂,B符合题意;
C. 氯化铁中铁元素化合价为+3价,具有强的氧化性,作氧化剂,C不符合题意;
D. 二氧化硅中硅元素的化合价为+4价,为硅元素的最高价态,具有氧化性,可用作氧化剂,D不符合题意;
故合理选项是B。

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
【题目】在密闭容器中发生下列反应:I2(g)+H2(g)![]() 2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
编号 | 改变的条件 | 反应速率 |
(1) | 升高温度 | ______ |
(2) | 加入正催化剂 | ______ |
(3) | 再充入a mol H2 | ______ |
(4) | 将容器的容积扩大到原来的2倍 | ______ |
(5) | 保持容积不变,通入b mol Ne | ______ |
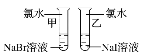
【题目】甲同学拟通过实验探究同主族元素性质的递变规律。其设计的实验方案如下,请你帮他填写完整,并做出评价。
实验室提供的试剂:NaBr溶液、NaI溶液、新制的氯水
(1)写出下列实验报告中的实验现象和离子方程式
实验步骤 | 实验现象 | 实验结论及离子方程式 |
| 甲_______ 乙_______ | 离子方程式 甲__________ 乙__________ 结论:卤素单质的氧化性由强到弱的顺序为Cl2>Br2>I2 |
(2)[评价]甲同学设计的实验方案的合理性是_____(填字母)。
A.非常合理 B.部分合理 C.完全不合理