题目内容
【题目】已知有A、B、C、D、E五种短周期的主族元素,它们的原子序数依次递增,A是所有元素中原子半径最小的元素,B、C组成的某一种化合物能引起温室效应。常温下,金属D单质投入水中能与水剧烈反应。常温下E单质是常见的气体。请按要求回答下列几个问题:
(1)B、D的元素名称分别为:________、________。
(2)E在周期表中的位置为:________。
(3)C离子的结构示意图为:________。
(4)B、C、D三种元素的原子半径从大到小的顺序为________(用元素符号表示)。
(5)B、E的最高价氧化物对应水化物的酸性从强到弱的顺序为:________(用对应的化学式表示)。
(6)写出C、D两种元素组成的阴、阳离子个数比为1:2且只含离子键的化合物的电子式:________。
【答案】碳 钠 第三周期第ⅤⅡA族 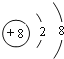 Na>C>O HClO4>H2CO3
Na>C>O HClO4>H2CO3 ![]()
【解析】
A、B、C、D、E五种短周期的主族元素,它们的原子序数依次递增,A是所有元素中原子半径最小的元素,则A为氢元素,B、C组成的某一种化合物能引起温室效应,则B为碳元素,C为氧元素,常温下,金属D单质投入水中能与水剧烈反应,且为短周期元素原子序数大于O,则D为钠元素,常温下E单质是常见的气体,E的原子序数大于钠,则E为氯元素。
(1)由上述分析可知,B、D的元素名称分别为碳元素和钠元素;
(2)E是氯元素,在周期表中第三周期第ⅤⅡA族;
(3)C为氧元素,氧离子的结构示意图为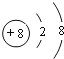 ;
;
(4)电子层数越多原子半径越大,电子层数相同原子序数越小半径越大,所以B、C、D三种元素的原子半径从大到小的顺序为Na>C>O;
(5)元素非金属性越强,对应的最高价氧化物对应水化物的酸性就越强,由于氯的非金属性强于碳,所以HClO4的酸性强于H2CO3;
(6)O和Na元素可以形成氧化钠,属于离子化合物,阴、阳离子个数比为1:2,只含有离子键,其电子式为![]() 。
。

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案【题目】由甲醇![]() 、氧气和
、氧气和![]() 溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
(1)写出该电池负极电极反应式______
(2)若以该电池为电源,用石墨作电极电解含有如下离子的溶液。
离子 |
|
|
|
|
|
|
|
|
|
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),阳极上发生的电极反应为______;阴极收集到的气体体积为(标准状况)______。
(3)若用该电池做电源,用石墨做电极电解硫酸铜溶液,当电路中转移![]() 时,实际上消耗的甲醇的质量比理论上大,可能原因是______。
时,实际上消耗的甲醇的质量比理论上大,可能原因是______。