题目内容
2.北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).丙烷脱氢可得丙烯.已知:C3H8(g)═CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ•mol-1;CH3CH=CH2(g)═CH4(g)+HC≡CH(g)△H2=32.4kJ•mol-1.则相同条件下,反应C3H8(g)═CH3CH=CH2(g)+H2(g)的△H=124.2kJ•mol-1.分析 根据盖斯定律,由已知热化学方程式乘以合适的系数进行加减构造目标目标热化学方程式,反应热也乘以相应的系数,进行相应的加减,据此计算;
解答 解:已知:①C3H8(g)═CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ•mol-1
②CH3CH=CH2(g)═CH4(g)+HC≡CH(g )△H2=32.4kJ•mol-1
根据盖斯定律,①-②得C3H8(g)═CH3CH=CH2(g)+H2(g),所以△H=△H1-△H2=156.6kJ•mol-1-32.4kJ•mol-1=124.2kJ•mol-1;
故答案为:124.2.
点评 本题考查反应热的计算,涉及盖斯定律的运用,注意目标热化学方程式的构建,难度中等.

练习册系列答案
相关题目
12.在N2+3H2?2NH3反应中,自反应开始至2s末,氨的浓度由0变为0.4mol•L-1,则以氢气的浓度变化表示该反应在2s内的平均反应速率是( )
| A. | 0.3 mol•L-1•s-1 | B. | 0.4 mol•L-1•s-1 | C. | 0.6 mol•L-1•s-1 | D. | 0.8 mol•L-1•s-1 |
17.在一定温度下的定容密闭容器中,当下列物理量不再改变时,表明反应:A(s)+2B(g)?C(g)+D(g) 已达平衡标志的是( )
| A. | 混合气体的密度 | B. | B物质的相对分子质量 | ||
| C. | 混合气体的压强 | D. | 气体的总物质的量 |
7.下列关于胶体的叙述不正确的是( )
| A. | 胶体区别于其他分散系的本质特征是分散质的微粒直径在1nm~100nm之间 | |
| B. | 用平行光照射CuSO4溶液和Fe(OH)3胶体,可以加以区分 | |
| C. | 把FeCl3饱和溶液滴入到NaOH溶液中,以制取Fe(OH)3胶体 | |
| D. | 树林中的晨曦,该现象与丁达尔效应有关 |
11.下列化学实验操作或事故处理方法不正确的是( )
| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸 | |
| C. | 酒精灯着火时可用湿布扑灭 | |
| D. | 蒸馏时,温度计水银球应浸没在液体中 |
12.对于反应2SO2+O2?2SO3,下列说法正确的是( )
| A. | 工业上常使用过量的空气,目的是为了使SO2的转化率达100% | |
| B. | 工业上选用V2O5作该反应的催化剂,目的是为了加快化学反应速率 | |
| C. | 工业上常选用常压,原因是增大压强不能改变该反应的化学反应速率 | |
| D. | 升高温度可以加快反应速率,所以在工业生产中该反应温度越高越好 |
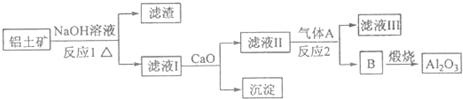
 (1)A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃性气体.而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊.D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体.请回答下列问题:
(1)A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃性气体.而C、D还生成一种无色无味气体H,该气体能使澄清石灰水变浑浊.D和A可反应生成C,F和H也可反应生成C和另一种无色无味气体.请回答下列问题: 具有的官能团有酯基和羧基(写名称).用阿司匹林和氢氧化钠中和制得可溶性阿司匹林,该反应的化学方程式为C6H5OOCCH3COOH+H2O→CH3COOH+C6H5OHCOOH.
具有的官能团有酯基和羧基(写名称).用阿司匹林和氢氧化钠中和制得可溶性阿司匹林,该反应的化学方程式为C6H5OOCCH3COOH+H2O→CH3COOH+C6H5OHCOOH.