题目内容
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.在密闭容器中加入l.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA |
| B.常温常压下,18g H2O含有的原子总数为3NA |
| C.1.0L的0.1 mol·L-1Na2S溶液中含有的S2-离子数为0.1NA |
| D.2SO2(g)+O2(g)=2SO3(g)和4SO2(g)+2O2(g)=4SO3(g)的△H相等 |
B
解析试题分析:A中H2和N2反应生成氨气的反应时可逆反应,l.5mol H2和0.5molN2充分反应后不可得到NH3分子数为NA,错误;B.常温常压下,18g H2O的物质的量是lmol,含有的原子总数为3NA;正确;C. 1.0L的0.1 mol·L-1Na2S溶液中S2-水解,含有的S2-离子数小于0.1NA,错误;D. 2SO2(g)+O2(g)=2SO3(g)和4SO2(g)+2O2(g)=4SO3(g)的△H后者是前者的2倍。所以,错误。
考点:阿伏伽德罗常数

练习册系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.1 mol N2所含有的原子数为NA |
| B.标准状况下,22.4 L水中含有的水分子数为NA |
| C.标准状况下,22.4 L氯化氢所含的原子数为NA |
| D.24 g O2分子和24 g O3分子所含的氧原子数目相等 |
下列有关化学用语正确的是( )
A.核内有8个中子的碳原子: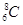 |
| B.CS2的结构式:S—C—S |
C.乙烯的比例模型: |
D.NH4Br的电子式: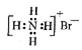 |
下列叙述不正确的是( )
A.用电子式表示HCl的形成过程: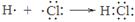 |
B.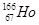 中的原子核内的中子数与核外电子数之差是99 中的原子核内的中子数与核外电子数之差是99 |
C.在空气中加热金属锂:4Li + O2 2Li2O 2Li2O |
D.铝热法炼铁:2Al + Fe2O3 2Fe+ Al2O3 2Fe+ Al2O3 |
化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
A.氢化铵的电子式: |
B.甲醇分子的球棍模型: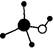 |
C.次氯酸分子的结构式: |
D.Ge原子结构示意图: |
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A.0.1mol的白磷(P4)或甲烷中所含的共价键数均为0.4NA |
| B.l L 0.1mol·L-1的H2SO3溶液中含有H+的数目为0.2NA |
| C.100mL 3 mol·L-1盐酸与11.2g Fe充分反应转移0.2NA个电子 |
| D.在标准状况下,22.4 L空气中约含有NA个气体分子 |
由硫酸钾、硫酸铝和硫酸组成的混合溶液,其c(H+)=0.1 mol·L-1,c(Al3+)=0.4 mol·L-1,c(SO42-)=0.8 mol·L-1,则c(K+)为
| A.0.15 mol·L-1 | B.0.2 mol·L-1 | C.0.3 mol·L-1 | D.0.4 mol·L-1 |
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.在反应5NH4NO3 2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA 2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA |
| B.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
| C.标准状况下,1.12L的SO3所含的原子数约为0.2NA |
| D.标准状况下,2.2gCO2气体中所含分子数为0.05NA |
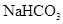 晶体中阳离子和阴离子总数为0.03NA ⑥3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA ⑦标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1NA
晶体中阳离子和阴离子总数为0.03NA ⑥3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA ⑦标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1NA