题目内容
设NA 表示阿伏加德罗常数,下列叙述中正确的是
①31g白磷含有的P—P键数为NA ② 1molCH3+(碳正离子)中含有电子数为10NA ③1mol铜与足量硫蒸气反应,转移电子数为2NA ④用惰性电极电解CuCl2溶液,阴极析出32g铜时,线路中通过的电子数为NA ⑤0.84 g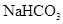 晶体中阳离子和阴离子总数为0.03NA ⑥3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA ⑦标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1NA
晶体中阳离子和阴离子总数为0.03NA ⑥3.9gNa2O2吸收足量的CO2时转移的电子数是0.05NA ⑦标准状况下,3.2g铜与足量的浓硝酸反应生成的气体含有的分子数是0.1NA
| A.①②④ | B.④⑥ | C.③④⑤ | D.④⑥⑦ |
B
解析试题分析:①白磷化学式P4,每摩尔的白磷中含有6NA的P—P键,n(P4)=m/M=31g÷124g/mol=0.25mol.故含有的P—P键为0.25 mol.×6=1.5NA。错误。每个CH3+(碳正离子)中含有电子数为8个,所以1molCH3+(碳正离子)中含有电子数为8NA.错误。③发生反应:2Cu+S Cu2S,所以1mol铜与足量硫蒸气反应,转移电子数为NA。错误。 ④用惰性电极电解CuCl2溶液,反应方程式为:CuCl2
Cu2S,所以1mol铜与足量硫蒸气反应,转移电子数为NA。错误。 ④用惰性电极电解CuCl2溶液,反应方程式为:CuCl2 Cu+Cl2.↑由方程式可看出,若转移电子2 NA,阴极析出铜1mol,即64g,。现在,线路中通过的电子数为NA,所以产生Cu32g.正确。 ⑤NaHCO3=Na++HCO3-。每摩尔的盐中含有2 NA个离子。n(NaHCO3)="m/M=0.84" g÷84g/mol=0.01mol.故晶体中阳离子和阴离子总数为0.02NA。错误。 ⑥Na2O2和CO2反应的方程式为:2Na2O2+2CO2= Na2CO3+O2.每摩尔的Na2O2反应,转移电子1mol.n(Na2O2)=" m/M=3.9g÷78g/mol=0.05mol" .所以转移的电子数是0.05NA 正确。⑦铜与足量的浓硝酸反应的方程式为:Cu+4HNO3(浓)= Cu(NO3)2+ 2NO2↑+2H2O. 2NO2
Cu+Cl2.↑由方程式可看出,若转移电子2 NA,阴极析出铜1mol,即64g,。现在,线路中通过的电子数为NA,所以产生Cu32g.正确。 ⑤NaHCO3=Na++HCO3-。每摩尔的盐中含有2 NA个离子。n(NaHCO3)="m/M=0.84" g÷84g/mol=0.01mol.故晶体中阳离子和阴离子总数为0.02NA。错误。 ⑥Na2O2和CO2反应的方程式为:2Na2O2+2CO2= Na2CO3+O2.每摩尔的Na2O2反应,转移电子1mol.n(Na2O2)=" m/M=3.9g÷78g/mol=0.05mol" .所以转移的电子数是0.05NA 正确。⑦铜与足量的浓硝酸反应的方程式为:Cu+4HNO3(浓)= Cu(NO3)2+ 2NO2↑+2H2O. 2NO2 N2O4.n(Cu) ="m/M=3.2g÷64g/mol=0.05mol" .3.2g铜与足量的浓硝酸反应生成的气体含有的分子数少于0.1NA。错误。
N2O4.n(Cu) ="m/M=3.2g÷64g/mol=0.05mol" .3.2g铜与足量的浓硝酸反应生成的气体含有的分子数少于0.1NA。错误。
考点:考查阿伏加德罗常数在物质结构、化学反应等计算中的应用的知识。

在一定温度下,已知有关某饱和溶液的一些数据:①溶液的质量,②溶剂的质量,③溶液的体积,④溶质的摩尔质量,⑤溶质的溶解度,⑥溶液的密度,利用下列各组数据计算该饱和溶液的物质的量浓度,不能算出的一组是( )
| A.④⑤⑥ | B.①②③④ | C.①④⑥ | D.①③④⑤ |
设NA代表阿伏加德罗常数,以下说法不正确的是( )。
| A.18 g水中含有电子数为10NA |
| B.16 g氧气所含原子数为NA |
| C.4.8 g金属镁变成镁离子时失去电子数为0.2NA |
| D.46 g二氧化氮和46 g四氧化二氮含有的原子数均是3NA |
下列溶液中的Na+与50 mL 1 mol·L-1 Na3PO3溶液中Na+的物质的量浓度相等的是
| A.150 mL 3 mol·L-1 NaCl溶液 | B.75 mL 2 mol·L-1 NaNO3溶液 |
| C.150 mL 2 mol·L-1 Na2SO4溶液 | D.75 mL 1 mol·L-1的Na2S溶液 |
用NA表示阿伏德罗常数,下列叙述正确的是
| A.标准状况下,22.4LH2O含有的分子数为1 NA |
| B.1.06g Na2CO3含有的Na+为0.02 NA |
| C.NA个CO2分子占有的体积为22.4L |
| D.物质的量浓度为0.5mol·/L的MgCl2溶液中,含有Cl- 1 NA |
设NA为阿佛加德罗常数的数值,下列说法正确的是( )
| A.常温常压下,8gO2含有4NA个电子 |
| B.1L0.1molL-1的氨水中有NA个NH4+ |
| C.标准状况下,22.4L盐酸含有NA个HCl分子 |
| D.1molNa被完全氧化生成Na2O2,失去个2NA电子 |
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.在密闭容器中加入l.5mol H2和0.5molN2,充分反应后可得到NH3分子数为NA |
| B.常温常压下,18g H2O含有的原子总数为3NA |
| C.1.0L的0.1 mol·L-1Na2S溶液中含有的S2-离子数为0.1NA |
| D.2SO2(g)+O2(g)=2SO3(g)和4SO2(g)+2O2(g)=4SO3(g)的△H相等 |
用NA表示阿伏加德罗常数的值。下列叙述中正确的是( )
| A.11.2g Fe投入到400mL 1mol/L的硝酸中充分反应,转移电子总数为0.2NA |
| B.标准状况下,11.2L C2H6含3NA个C—H极性共价键 |
| C.标准状况下,5.6 L NO和5.6 L O2混合后的分子总数为0.5 NA |
| D.标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA |
同温同压下,等容积的两容器内分别充满14N18O和13C18O气体。下列说法正确的是
| A.所含分子数和质量均不相同 | B.含有相同的分子数和电子数 |
| C.含有相同的质子数和中子数 | D.含有相同数目的中子、原子和分子 |