��Ŀ����
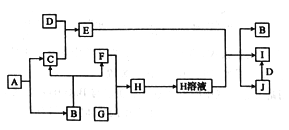
����Ŀ��ij������Ա��Ƴ�������������Ҫ�ɷ�Fe2O3������������SiO2�����ʣ������õ����̡������е���Һ�������ѭ�������������Ʊ���������ĩ��


��1��Ϊ�˼ӿ췴Ӧ���ķ�Ӧ���ʣ��ɲ��õĴ�ʩ�� ����д��һ�㼴�ɣ�
��2������ԭ���ǽ�Fe3��ת��ΪFe2�������¶�T1 ��T2��T1 ��T2���½��и÷�Ӧ��ͨ�������ͬʱ������Һ��pH������pH��ʱ��ı仯��������ͼ��ʾ���ó����ۣ��÷�Ӧ���¶Ȳ��˹��ߡ�
��ͨ��SO2��������ԭ��ʱ�� �Խ���pH�½���ԭ���� ��
����ͬʱ���ڣ�T1�¶�����Һ��pH���ߵ�ԭ���� ��
��3����������ѭ��ʹ�õ������� ��
��4��Ϊ�ⶨ��Ӧ������Һ��Fe3����Ũ���Կ��Ƽ���SO2������ʵ�鲽��Ϊ��ȷ��ȡ20.00ml�ķ�Ӧ����Һ��ϡ�ͳ�100mL��Һ��ȡ10.00 mL��Һ������������KI�����2��3�ε�����Һ����0.50mol/L��Na2S2O3��Һ��ⷴӦ������Ӧǡ����ȫ����ʱ��������Na2S2O3��Һ20.00 mL���йط�Ӧ����ʽ���£�2Fe3����2I����2Fe2����I2�� 2Na2S2O3 + I2�� Na2S4O6 + 2NaI
�Լ���ԭ��Һ��Fe3�������ʵ���Ũ��(д���������)��
���𰸡���1�������������顢�ʵ����������Ũ�ȡ������¶ȡ�����ȣ�
��2����Fe3����SO2��ˮ��Һ��H2SO3������ΪH2SO4�����¶ȹ��ߣ� SO2���ܽ���½���
��3��H2SO4 ��
��4���ɷ�Ӧʽ�ɵù�ϵ��Fe3����Na2S2O3
n(Fe3��)=n(Na2S2O3)=20.00��10-3L��0.50mol/L��10=0.1 mol��
�� c(Fe3��)= ![]() =5��0mol/L��
=5��0mol/L��
�������������������1�����Ӱ�췴Ӧ���ʵ����أ�����������ʱ����ͨ��������顢�����¶ȡ����衢��������Ũ������߷�Ӧ���ʣ��ʴ�Ϊ�������������顢�ʵ����������Ũ�ȡ������¶ȡ�����ȣ�
��2����Fe3+��SO2��ˮ��Һ��H2SO3������ΪH2SO4������Һ��pH�����٣�Ҳ������Һ��������ǿ���ʴ�Ϊ��Fe3+��SO2��ˮ��Һ��H2SO3������ΪH2SO4��
���¶����ߣ����Լӿ췴Ӧ���ʣ���������ܽ��ȴ��С�ˣ��μӷ�Ӧ��SO2�������٣�����ͬʱ���ڣ�T1�¶�����Һ��pH���ߣ��ʴ�Ϊ���¶ȹ��ߣ�SO2���ܽ���½���
��3��������ͼ�пɿ�������ѭ�����õ�������H2SO4���ʴ�Ϊ��H2SO4��
��4���ɷ�Ӧʽ�ɵù�ϵ��Fe3+��Na2S2O3��n��Fe3+��=n��Na2S2O3��=20.00��10-3L��0.50mol/L��10=0.1 mol��c��Fe3+��=![]() =5.0mol/L����ԭ��Һ������Ũ��Ϊ5.0mol/L��
=5.0mol/L����ԭ��Һ������Ũ��Ϊ5.0mol/L��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�