题目内容
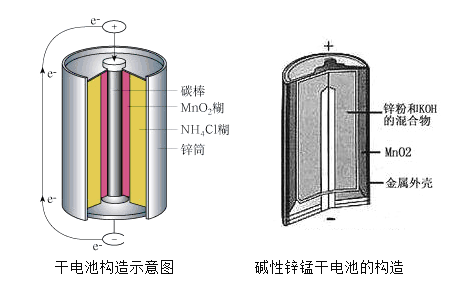
【题目】锌锰电池在生活中的用量很大。酸性锌锰电池(干电池)和碱性锌锰电池的构造如图所示。下列有关说法错误的是( )
A. 二者分别消耗6.5g锌,都将转移0.2mol电子
B. 二者的正极反应式均为![]()
C. 碱性锌锰电池比酸性锌锰电池比能量高
D. 酸性锌锰电池易发生漏液现象
【答案】B
【解析】
A.二者的负极皆为Zn,负极锌失电子,所以消耗6.5g锌,都将转移0.2mol电子,故A正确;
B.酸性锌锰电池的正极反应式为MnO2 + H+ + e = MnO(OH) 或MnO2 +NH4+ + e = MnO(OH) +NH3碱性锌锰电池正极反应式为MnO2 + H2O + e = MnO(OH) + OH ,故B错误;
C.电池的比能量就是参与电极反应的单位质量的电极材料放出电能的大小。碱性锌锰电池的电极材料分别采用锌粉、MnO2,而酸性锌锰电池采用锌筒、MnO2和石墨,所以前者比能量高,故C正确;
D.NH4Cl糊呈酸性,锌筒会被其腐蚀而发生漏液现象,故D正确。选B。

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目