题目内容
8.下列对于“物质的量”或“摩尔”的理解正确的是( )| A. | 物质的量是国际科学界建议采用的一种物理量 | |
| B. | 物质的量是摩尔的单位,符号为n | |
| C. | 摩尔可以把物质的宏观数量与微观粒子的数量联系起来的物理量 | |
| D. | 国际上规定,0.012kg碳原子所含有的碳原子数目为1mol |
分析 A.物质的量是一种物理量;
B.物质的量的单位摩尔其符号为mol;
C.物质的量是把物质的宏观数量与微观粒子的数量联系起来的物理量;
D.是以12C所含有的碳原子数为标准.
解答 解:A.物质的量是一种物理量,是国际科学界建议采用的一种物理量,故A正确;
B.物质的量的单位摩尔其符号为mol,物质的量的符号为n,故B错误;
C.物质的量是把物质的宏观数量与微观粒子的数量联系起来的物理量,摩尔是物质的量的单位,不是物理量,故C错误;
D.是以12C所含有的碳原子数为标准,即0.012kg12C所含有的碳原子数目为1mol,故D错误.
故选A.
点评 本题考查了物质的量及其单位,掌握摩尔物质的量的单位、摩尔是单位不是物理量、使用摩尔时基本微粒应予指明等是正确解答本题的关键,题目难度不大.

练习册系列答案
相关题目
19.相同物质的量浓度、相同体积的KOH溶液,分别与相同体积的Fe2(SO4)3溶液和FeSO4溶液反应,要使溶液中的Fe3+、Fe2+恰好完全沉淀,则FeSO4溶液和Fe2(SO4)3溶液的物质的量浓度之比为( )
| A. | 3:2 | B. | 3:1 | C. | 1:3 | D. | 1:1 |
16.2.8g Fe全部溶于一定浓度、200mL的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1.若反应前后溶液体积变化忽略不计,则下列有关判断正确的是( )
| A. | 反应后的溶液最多还能溶解1.4 g Fe | |
| B. | 反应后溶液中c(NO3-)=0.85 mol/L | |
| C. | 反应后溶液中铁元素可能以Fe2+形式存在 | |
| D. | 1.12 L气体可能是NO、NO2的混合气体 |
3.有2mol过氧化钠与3mol碳酸氢钠的固体混合物,在密闭容器中加热充分反应,排出气体物质后冷却,下列有关残留的固体物质和排出的气体的说法中正确的是( )
| A. | 残留的固体物质为Na2CO3 | |
| B. | 残留的固体物质0.5molNa2O2,1molNa2CO3 | |
| C. | 排出的气体为1molO2,并无H2O(g) | |
| D. | 排出的气体为1molO2,1molH2O(g) |
20.下列实验操作中,正确的是( )
| A. | 蒸发时垫石棉网可以防止蒸发皿因受热不均匀炸裂 | |
| B. | 酒精灯熄灭点火时可用打火机,熄灭时可轻轻吹灭 | |
| C. | 试管内壁附着的沉淀物一般用盐酸洗涤 | |
| D. | 过滤后洗涤一般2~3次,所加蒸馏水不宜过多 |
8.亚氯酸钠(NaClO2)常用于水的消毒和砂糖、油脂的漂白与杀毒.以下是用过氧化氢法生产亚氯酸钠的工艺流程图1:
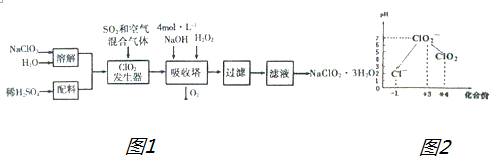
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O
②Ksp(FeS)=6.3×10-18;Ksp(CuS)=6.3×10-20;Ksp(PbS)=2.4×10-28
(1)吸收塔内发生反应的离子方程式为2OH-+2ClO2+H2O2═2ClO2-+O2↑+2H2O.
(2)从滤液中得到NaClO2•3H2O晶体的所需操作依次是edcf(填写序号).
a.蒸馏 b.灼烧 c.过滤 d.冷却结晶 e.加热蒸发 f.洗涤干燥
(3)自来水厂也可用ClO2消毒杀菌,处理后的水中要求ClO2的浓度在0.1~0.8mg•L-1之间.碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝.
Ⅱ.加入一定量的Na2S2O3溶液进行滴定,发生2S2O32-+I2═S4O62-+2I-反应.
Ⅲ.加硫酸调节水样pH至1~3.操作时,不同pH环境中粒子种类如图2所示;请回答:
①操作Ⅱ滴定终点的现象是溶液蓝色刚好褪去,且保持30秒不变色.
②在操作Ⅱ过程中,溶液又呈蓝色,反应的离子方程式是ClO2-+4I-+4H+=Cl-+2I2+2H2O.
③若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10-3mol/LNa2S2O3溶液8ml,则水样中ClO2的浓度为0.54mg/L.
(4)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2.
下表是25℃时HClO2及几种常见弱酸的电离平衡常数:
①常温下,物质的量浓度相等的NaClO2、NaF、NaCN、Na2S四种溶液的pH由大到小的顺序为pH(Na2S)>pH(NaCN)>pH(NaF)>pH(NaClO2)(用化学式表示);体积相等,物质的浓度相同的NaF、NaCN两溶液中所含阴阳离子总数的大小关系为:前者大(填“前者”“相等”或“后者大”).
②Na2S是常用的沉淀剂,某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是CuS;当最后一种离子沉淀完全时,此时体系中的S2-的浓度为6.3×10-13mol/L.

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O
②Ksp(FeS)=6.3×10-18;Ksp(CuS)=6.3×10-20;Ksp(PbS)=2.4×10-28
(1)吸收塔内发生反应的离子方程式为2OH-+2ClO2+H2O2═2ClO2-+O2↑+2H2O.
(2)从滤液中得到NaClO2•3H2O晶体的所需操作依次是edcf(填写序号).
a.蒸馏 b.灼烧 c.过滤 d.冷却结晶 e.加热蒸发 f.洗涤干燥
(3)自来水厂也可用ClO2消毒杀菌,处理后的水中要求ClO2的浓度在0.1~0.8mg•L-1之间.碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝.
Ⅱ.加入一定量的Na2S2O3溶液进行滴定,发生2S2O32-+I2═S4O62-+2I-反应.
Ⅲ.加硫酸调节水样pH至1~3.操作时,不同pH环境中粒子种类如图2所示;请回答:
①操作Ⅱ滴定终点的现象是溶液蓝色刚好褪去,且保持30秒不变色.
②在操作Ⅱ过程中,溶液又呈蓝色,反应的离子方程式是ClO2-+4I-+4H+=Cl-+2I2+2H2O.
③若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10-3mol/LNa2S2O3溶液8ml,则水样中ClO2的浓度为0.54mg/L.
(4)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2.
下表是25℃时HClO2及几种常见弱酸的电离平衡常数:
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka/mol•L-1 | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-12 |
②Na2S是常用的沉淀剂,某工业污水中含有等浓度的Cu2+、Fe2+、Pb2+离子,滴加Na2S溶液后首先析出的沉淀是CuS;当最后一种离子沉淀完全时,此时体系中的S2-的浓度为6.3×10-13mol/L.
9.化学与生活密切相关.下列应用中利用了物质氧化性的是( )
| A. | 漂白粉漂白织物 | B. | 纯碱去油污 | C. | 食醋除水垢 | D. | 明矾净化水 |