题目内容
【题目】LiH在熔融状态下能导电。有关分析错误的是
A. 原子半径:Li>H B. 两者都是第IA族元素
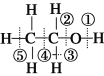
C. 离子半径:Li+>H- D. 电子式:![]()
【答案】C
【解析】
LiH在熔融状态下能导电,属于离子化合物;锂原子、氢原子最外层电子数均为1,都属于IA族元素;同一主族元素从上到下,原子半径增大;核外电子排布相同的离子,核电荷数越大,离子半径越小,据此进行分析。
LiH在熔融状态下能导电,属于离子化合物;锂原子、氢原子最外层电子数均为1,都属于IA族元素,
A. 两种元素位于同一主族,从上到下,原子半径逐渐增大,因此原子半径:Li>H,A正确;
B. 两原子最外层电子数均为1,都是第IA族元素,B正确;
C. 核外电子排布相同的离子,核电荷数越大,离子半径越小,因此离子半径Li+<H-,C错误;
D. LiH在熔融状态下能导电,属于离子化合物,其电子式:![]() ,D正确;
,D正确;
综上所述,本题选C。

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目