题目内容
离子化合物AB2的阴、阳离子的电子层结构相同,1 mol AB2中含54 mol电子,且有下列反应:
①H2+B2 C
C
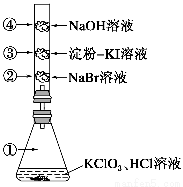
②B2+X→Y+AB2+H2O
③Y+C→AB2+Z,Z有漂白作用。
根据上述条件回答下列问题:
(1)写出下列物质的化学式:AB2__________,X________,Y________,Z________。
(2)用电子式表示AB2的形成过程:_____________________________________________。
(3)写出反应②的化学方程式:______________________________________。
(1)CaCl2 Ca(OH)2 Ca(ClO)2 HClO
(2)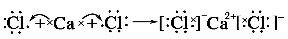
(3)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
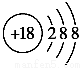
【解析】由题目信息可知:在离子化合物中A2+、B-核外电子数均为18个,则元素A、B分别是Ca和Cl。
再由化学反应“H2+Cl2―→C”推出C为HCl;因为反应②:Cl2+X―→Y+CaCl2+H2O,可推知X中含有元素Ca、H、O。则X可能是Ca(OH)2,则反应②为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。最后反应③为:Ca(ClO)2+2HCl=CaCl2+2HClO。

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目