题目内容
某有机物的结构简式是: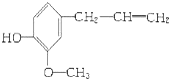 该物质不应有的化学性质是( )
该物质不应有的化学性质是( )
①可以燃烧
②可以跟溴加成
③可以将KMnO4酸性溶液还原
④可以跟NaHCO3溶液反应
⑤可以跟NaOH溶液反应
⑥可以发生消去反应.
 该物质不应有的化学性质是( )
该物质不应有的化学性质是( )①可以燃烧
②可以跟溴加成
③可以将KMnO4酸性溶液还原
④可以跟NaHCO3溶液反应
⑤可以跟NaOH溶液反应
⑥可以发生消去反应.
| A、①③ | B、③⑥ | C、④⑥ | D、④⑤ |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:由结构简式可知,分子中含酚-OH、碳碳双键及醚键,结合酚、烯烃的性质来解答.
解答:
解:①为烃的含氧衍生物,可以燃烧生成二氧化碳和水,故不选;
②含碳碳双键,可以跟溴发生加成反应,故不选;
③含碳碳双键,可以将KMnO4酸性溶液还原,故不选;
④酚-OH的酸性很弱,不能跟NaHCO3溶液反应,故选;
⑤含酚-OH,可以跟NaOH溶液反应,故不选;
⑥酚-OH不能发生消去反应,故选;
故选C.
②含碳碳双键,可以跟溴发生加成反应,故不选;
③含碳碳双键,可以将KMnO4酸性溶液还原,故不选;
④酚-OH的酸性很弱,不能跟NaHCO3溶液反应,故选;
⑤含酚-OH,可以跟NaOH溶液反应,故不选;
⑥酚-OH不能发生消去反应,故选;
故选C.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚和烯烃性质的考查,注意能发生消去反应的官能团及结构特点,题目难度不大.

练习册系列答案
相关题目
下列离子方程式正确的是( )
| A、NO2通入AgNO3溶液中:3NO2+H2O=2NO3-+NO+2H+ |
| B、过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O |
| C、过量NaOH滴入NH4HCO3稀溶液中:NH4++OH-═NH3?H2O |
| D、铜片加入稀HNO3中:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
分子式为C6H12O2的有机物,已知它在NaOH溶液及在稀硫酸中均能发生反应,则符合此条件的该有机物最多有( )
| A、20种 | B、9种 |
| C、7种 | D、25种 |
根据如图回答,下列说法不正确的是( )


| A、此装置用于电镀铜时,电解一段时间,硫酸铜溶液浓度不变 |
| B、燃料电池中正极反应为O2+4e-+4H+═2H2O |
| C、若a为粗铜,b为纯铜,该装置可用于粗铜的精炼 |
| D、电子经导线流入a电极 |
下列选项中所涉及的两个量一定相等的是( )
| A、电解精炼铜时阳极溶解与阴极析出的铜的质量 |
| B、6.29 Na2O 和7.89 Na2O2中所含的离子数 |
| C、11.2L N2与14g CO气体所含有的原子数 |
| D、20g重水(D2O)与34g NH3所含有的电子数 |
加成反应是有机化学中的一类重要的反应,下列属于加成反应的是( )
| A、甲烷与氯气混合后光照反应 |
| B、植物油通过氢化反应制人造脂肪源 |
| C、乙烯使酸性高锰酸钾溶液褪色 |
| D、在苯中滴入溴水,溴水褪色 |
对下列事实的解释正确的是( )
| A、常温下,将铜放入浓硫酸中无明显变化,说明铜在冷的浓硫酸中钝化 |
| B、向某溶液中加入氯化钡溶液和稀硝酸,生成白色沉淀,则原溶液一定含有SO42- |
| C、在蔗糖中加入浓H2SO4后出现发黑现象,说明浓H2SO4具有脱水性 |
| D、某红棕色气体通入中,水溶液为酸性,说明该气体为NO2 |
若要将0.6mol甲烷完全和氯气发生取代反应,并且生成相同物质的量的四种取代物,则需要氯气的物质的量为( )
| A、2.5 mol |
| B、4.5 mol |
| C、0.6 mol |
| D、1.5 mol |
向1mL 0.5mol?L-1 AlCl3溶液中加入3mL饱和NaF溶液,再加入1mL 3mol?L-1氨水,没有生成白色沉淀,其最主要的原因是( )
| A、3mol?L-1氨水的浓度不够大,溶液的碱性不够强 |
| B、NaF溶液碱性较强,Al3+完全反应生成AlO2-,而AlO2-不能与氨水反应生成Al(OH)3 |
| C、氨水为弱碱溶液,Al3+不与弱碱反应 |
| D、Al3+与F-结合生成新物质,溶液中几乎没有Al3+ |